题目内容
铁丝与氧气或水蒸气反应的共同产物是( )
| A、FeO |
| B、Fe3O4 |
| C、Fe2O3 |
| D、Fe2O3和Fe3O4 |
考点:铁的化学性质
专题:元素及其化合物
分析:铁丝在氧气中燃烧生成四氧化三铁,红热的铁与水蒸气反应生成四氧化三铁和氢气,以此来解答.
解答:
解:铁丝在氧气中燃烧3Fe+2O2
Fe3O4,生成四氧化三铁;红热的铁与水蒸气反应3Fe+4H2O(g)
Fe3O4+4H2,生成四氧化三铁和氢气,则共同产物为四氧化三铁(Fe3O4),
故选:B.
| ||
| ||
故选:B.
点评:本题考查铁的化学性质,明确发生的化学反应为解答的关键,注意Fe能在纯氧中燃烧,不能在空气中燃烧,把握发生的氧化还原反应即可解答,题目难度不大.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
下列物质不是生活中常用的添加剂的是( )
| A、食盐 | B、面粉 | C、酱油 | D、味精 |
某有机物是药物生产的中间体,其结构如图.下列有关叙述不正确的是( )
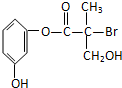

| A、该有机物与浓溴水可发生取代反应,1 mol该有机物可消耗3 mol溴 |
| B、该有机物与浓硫酸混合共热可发生消去反应 |
| C、1 mol该有机物与足量NaOH溶液反应最多消耗4 mol NaOH |
| D、1 mol该有机物催化加氢最多消耗3 mol氢气 |
2SO2(g)+O2(g)?2SO3(g)是工业制硫酸的主要反应之一.一定温度下,在甲、乙、丙三个容积均为2L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示.下列判断中,正确的是( )
| 甲 | 乙 | 丙 | ||
| 起始物质的量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | |
| SO2的平衡转化率/% | 80 | α1 | α2 | |
| A、甲中反应的平衡常数小于乙 |
| B、该温度下,平衡常数值为400 |
| C、平衡时,丙中c(SO3)是甲中的2倍 |
| D、平衡时,甲中O2的转化率大于乙中O2的转化率 |
固体氧化物燃料电池(SOFC)以固体氧化物作为电解质.其工作原理如图所示:下列关于固体燃料电池的有关说法正确的是( )
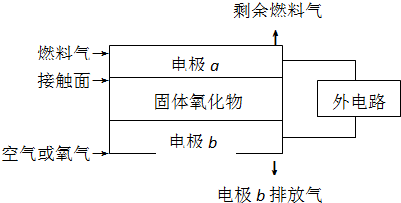

| A、电极b为电池负极,电极反应式为2O2+4e-=4O2- |
| B、固体氧化物的作用是让电子在电池内通过 |
| C、若H2作为燃料气,则接触面上发生的反应为H2+2OH--4e-=2H++H2O |
| D、若C2H4作为燃料气,则接触面上发生的反应为C2H4+6O2--12e-=2CO2+2H2O |
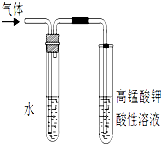 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.