题目内容
依据事实,写出下列反应的热化学方程式.
(1)已知稀溶液中,1mol H2SO4与 NaOH 恰好完全反应时,放出 114.6kJ热量,写出表示H2SO4与NaOH反应生成 1molH2O 的热化学方程式: .
(2)25℃、101kPa 条件下充分燃烧一定量的丁烷气体放出热量为 Q kJ,经测定,将生成的 CO2 通入足量澄清石灰水中产生 25g 白色沉淀,写出表示丁烷燃烧热的热化学方程式 .
(3)已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为 .
(4)已知:下列两个热化学方程式:
Fe(s)+
O2(g)═FeO(s)?△H=-272.0KJ/mol
2Al(s)+
O2(g)═Al2O3(s)?△H=-1675.7KJ/mol
则 Al(s)的单质和FeO(s)反应的热化学方程式是 .
(1)已知稀溶液中,1mol H2SO4与 NaOH 恰好完全反应时,放出 114.6kJ热量,写出表示H2SO4与NaOH反应生成 1molH2O 的热化学方程式:
(2)25℃、101kPa 条件下充分燃烧一定量的丁烷气体放出热量为 Q kJ,经测定,将生成的 CO2 通入足量澄清石灰水中产生 25g 白色沉淀,写出表示丁烷燃烧热的热化学方程式
(3)已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
(4)已知:下列两个热化学方程式:
Fe(s)+
| 1 |
| 2 |
2Al(s)+
| 3 |
| 2 |
则 Al(s)的单质和FeO(s)反应的热化学方程式是
考点:热化学方程式
专题:化学反应中的能量变化
分析:(1)依据中和热的概念是强酸强碱的稀溶液完全反应生成1mol水放出的热量,标注物质聚集状态和对应反应焓变得到;
(2)根据生成碳酸钙的质量计算丁烷的物质的量,结合燃烧热的概念书写表示丁烷燃烧热化学方程式;
(3)化学反应中,化学键断裂吸收能量,形成新化学键放出能量,根据方程式计算分别吸收和放出的能量,以此计算反应热并判断吸热还是放热;
(4)依据题干热化学方程式结合盖斯定律写出该热化学反应方程式.
(2)根据生成碳酸钙的质量计算丁烷的物质的量,结合燃烧热的概念书写表示丁烷燃烧热化学方程式;
(3)化学反应中,化学键断裂吸收能量,形成新化学键放出能量,根据方程式计算分别吸收和放出的能量,以此计算反应热并判断吸热还是放热;
(4)依据题干热化学方程式结合盖斯定律写出该热化学反应方程式.
解答:
解:(1)1mol H2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,H2SO4与NaOH反应的中和热的热化学方程式为:
H2SO4(aq)+NaOH(aq)=Na2SO4(aq)+H2O(l)△H=-57.3kJ?mol-1故答案为:
H2SO4(aq)+NaOH(aq)═
Na2SO4(aq)+H2O(l)△H=-57.3 kJ/mol;
(2)(2)n(CaCO3)=
=0.25mol,
Ca(OH)2+CO2=CaCO3+H2O
1 1
0.25mol 0.25mol
即丁烷燃烧生成的二氧化碳为0.25mol.
2C4H10+13O2=8CO2+10H2O
2 8
x 0.25mol
x=
mol=
mol
因为燃烧
mol的丁烷放出的热量为Q,则丁烷的燃烧热为16Q,所以表示丁烷燃烧热化学方程式为 C4H10(g)+
O2(g)=4CO2(g)+5H2O(l)△H=-16QkJ/mol,
故答案为:C4H10(g)+
O2(g)=4CO2(g)+5H2O(l)△H=-16QkJ/mol;
(3)在反应N2+3H2?2NH3中,断裂3molH-H键,1mol N三N键共吸收的能量为:3×436kJ+946kJ=2254kJ,生成2mol NH3,共形成6mol N-H键,放出的能量为:6×391kJ=2346kJ,吸收的能量少,放出的能量多,该反应为放热反应,放出的热量为:2346kJ-2254kJ=92kJ,
故答案为:N2(g)+3H2(g)═2NH3(g)△H=-92KJ/mol;
(4)①Fe(s)+
O2(g)=FeO(s)△H=-272.0kJ?mol-1
②2Al(s)+
O2(g)=Al2O3(s)△H=-1675.7kJ?mol-1
将方程式②-①×3得2Al(s)+3FeO(s)═Al2O3(s)+3Fe(s)△H=-859.7 kJ?mol-1,
故答案为:2Al(s)+3FeO(s)═Al2O3(s)+3Fe(s)△H=-859.7 kJ?mol-1.
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
(2)(2)n(CaCO3)=
| 25g |
| 100g/mol |
Ca(OH)2+CO2=CaCO3+H2O
1 1
0.25mol 0.25mol
即丁烷燃烧生成的二氧化碳为0.25mol.
2C4H10+13O2=8CO2+10H2O
2 8
x 0.25mol
x=
| 2×0.25 |
| 8 |
| 1 |
| 16 |
因为燃烧
| 1 |
| 16 |
| 13 |
| 2 |
故答案为:C4H10(g)+
| 13 |
| 2 |
(3)在反应N2+3H2?2NH3中,断裂3molH-H键,1mol N三N键共吸收的能量为:3×436kJ+946kJ=2254kJ,生成2mol NH3,共形成6mol N-H键,放出的能量为:6×391kJ=2346kJ,吸收的能量少,放出的能量多,该反应为放热反应,放出的热量为:2346kJ-2254kJ=92kJ,
故答案为:N2(g)+3H2(g)═2NH3(g)△H=-92KJ/mol;
(4)①Fe(s)+
| 1 |
| 2 |
②2Al(s)+
| 3 |
| 2 |
将方程式②-①×3得2Al(s)+3FeO(s)═Al2O3(s)+3Fe(s)△H=-859.7 kJ?mol-1,
故答案为:2Al(s)+3FeO(s)═Al2O3(s)+3Fe(s)△H=-859.7 kJ?mol-1.
点评:本题考查了盖斯定律的应用以及热化学方程式的书写知识,注意知识的归纳和整理是关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列离子方程式正确的是( )
| A、FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+═4Fe3++2H2O | ||||
| B、过量石灰水与碳酸氢钙反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | ||||
C、H
| ||||
| D、向氯化铝溶液中滴加过量氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
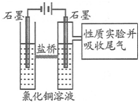 利用如图装置作电解50mL 0.5mol/L的CuCl2溶液实验.
利用如图装置作电解50mL 0.5mol/L的CuCl2溶液实验.