题目内容
13.有A、B、C、D、E、F六种短周期元素,他们的原子序数依次增大,B与A能以原子个数1:1、1:2、1:3或1:4等比值组成多种常见化合物;C的最髙正价和最低负价的代数和为2:A与E位于同一主族;D与F位于同一主族,且F的质子数是D的2倍;D与E能以原子个数1:1或1:2形成两种常见化合物.请根据题意完成以下空白:(1)F在元素周期表中的位置为第三周期第VIA族..
(2)A与B能形成一种最简单的直线型分子,其电子式为H:C┇┇C:H.
(3)CA3极易溶于液态A2D中,其原因是NH3和H2O都为极性分子,相似相溶、NH3分子和H2O分子间易形成氢键.
(4)将标准状况下的4.48L CA3完全溶解在含有O.1molHCl的水溶液中得1L溶液,测得所得溶液的pH=9,在该溶液中离子浓度由大到小的顺序为c(NH4+)>c(Cl-)>c(OH-)>c(H+).
(5)物质BA3BA2DA在电解质EDA的溶液作用下,可形成燃料电池,则该燃料电池的负极反应式为CH3CH2OH-12e-+16OH-=2CO32-+11H2O
(6)新型的BA3BA2DA燃料电池,它是用碘酸类质子溶剂,在2000C左右时供电,其效率比甲醇燃料电池高出32倍,且更安全.则该燃料电池的负极反应式为CH3CH2OH-12e-+3H2O=2CO2+12H+
(7)E与F形成的化合物在固态时属于离子晶体,用惰性电极电解该化合物的水溶液时,有固体析出,则该电解总反应方程式为Na2S+2H2O$\frac{\underline{\;通电\;}}{\;}$S↓+2NaOH+H2↑.
分析 有A、B、C、D、E、F六种短周期元素,他们的原子序数依次增大,B与A能以原子个数1:1、1:2、1:3或1:4等比值组成多种常见化合物,则A是H、B是C元素;A与E位于同一主族,D与E能以原子个数1:1或1:2形成两种常见化合物,则E是Na元素;
C的最髙正价和最低负价的代数和为2,原子序数小于E,则C为N元素;
D与F位于同一主族,且F的质子数是D的2倍,则D是O元素、F为S元素,结合题目分析解答.
解答 解:有A、B、C、D、E、F六种短周期元素,他们的原子序数依次增大,B与A能以原子个数1:1、1:2、1:3或1:4等比值组成多种常见化合物,则A是H、B是C元素;A与E位于同一主族,D与E能以原子个数1:1或1:2形成两种常见化合物,则E是Na元素;
C的最髙正价和最低负价的代数和为2,原子序数小于E,则C为N元素;
D与F位于同一主族,且F的质子数是D的2倍,则D是O元素、F为S元素;
(1)F是S元素,位于第三周期第VIA族,故答案为:第三周期VIA族;
(2)A是H、B是C元素,二者形成的直线形物质是乙炔,其电子式为H:C┇┇C:H,故答案为:H:C┇┇C:H;
(3)NH3极易溶于液态H2O中,氨气和水分子之间易形成氢键而导致氨气易溶于水,氨气和水都是极性分子导致氨气易溶于水,
故答案为:NH3和H2O都为极性分子,相似相溶;NH3分子和H2O分子间易形成氢键;
(4)将标准状况下的4.48L NH3完全溶解在含有0.1molHCl的水溶液中得1L溶液,氨气的物质的量是0.2mol,混合溶液中溶质为等物质的量浓度的氨水和氯化铵,测得所得溶液的pH=9,说明一水合氨电离程度大于铵根离子水解程度,结合电荷守恒得c(NH4+)>c(Cl-),在该溶液中离子浓度由大到小的顺序为c(NH4+)>c(Cl-)>c(OH-)>c(H+),
故答案为:c(NH4+)>c(Cl-)>c(OH-)>c(H+);
(5)物质CH3CH2OH在电解质NaOH的溶液作用下,可形成燃料电池,负极上乙醇失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为CH3CH2OH-12e-+16OH-=2CO32-+11H2O,
故答案为:CH3CH2OH-12e-+16OH-=2CO32-+11H2O;
(6)新型的CH3CH2OH燃料电池,它是用碘酸类质子溶剂,在2000C左右时供电,其效率比甲醇燃料电池高出32倍,且更安全,该燃料电池是酸性燃料电池,负极上乙醇失电子和水反应生成二氧化碳和氢离子,则该燃料电池的负极反应式为CH3CH2OH-12e-+3H2O=2CO2+12H+,
故答案为:CH3CH2OH-12e-+3H2O=2CO2+12H+;
(7)Na与S形成的化合物在固态时属于离子晶体,用惰性电极电解该化合物的水溶液时,有固体析出,为S单质,阴极上氢离子放电生成氢气,则该电解总反应方程式为Na2S+2H2O$\frac{\underline{\;通电\;}}{\;}$S↓+2NaOH+H2↑,
故答案为:离子;Na2S+2H2O$\frac{\underline{\;通电\;}}{\;}$S↓+2NaOH+H2↑.
点评 本题考查位置结构性质相互关系及应用,为高频考点,涉及元素推断、元素周期律、盐类水解、原电池和电池原理等知识点,明确元素周期律、盐的性质、原电池和电解池原理是解本题关键,难点是电极反应式的书写,题目难度中等.

(1)对PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol.L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料.已知:H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-241.8KJ/mol
C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-110.5KJ/mol
写出焦炭与水蒸气反应的热化学方程式C(s)+H2O(g)=CO(g)+H2(g)H=+131.3KJ/mol;
②洗涤含SO2的烟气,以下物质可作洗涤剂的是ab;
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)汽车尾气中NOx和CO的生成及转化为:
①已知气缸中生成NO的反应为:N2(g)+O2(g)?2NO(g)△H>0
若1mol空气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡.测得NO为8×10-4mol.计算该温度下的平衡常数K=4×10-6;汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是因为该反应为吸热反应,温度越高,反应速率加快,平衡右移.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:
2CO(g)=2C(s)+O2(g)已知该反应的△H>0,简述该设想能否实现的依据该反应是焓增,熵减的反应,任何温度下均不自发进行.
③目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2.
(2)量取反应物时,取50mL 0.50mol•L-1的盐酸,还需加入的试剂是B.
A.50mL 0.50mol•L-1 NaOH溶液 B.50mL 0.55mol•L-1 NaOH溶液
C.1.0g NaOH固体
(3)实验时大烧杯上若不盖硬纸板,求得的中和热数值偏小(填偏大、偏小、无影响)
(4)由甲、乙两人组成的实验小组,在同样的实验条件下,用同样的实验仪器和方法进行两组测定中和热的实验,实验试剂及其用量如表所示.
| 反应物 | 起始温度t1/℃ | 终了温度t2/℃ | 中和热/kJ•mol-1 |
| A.1.0mol/L HCl溶液50mL、1.1mol/L NaOH溶液50mL | 13.0 | 19.8℃ | △H1 |
| B.1.0mol/L HCl溶液50mL、1.1mol/L NH3•H2O溶液50mL | 13.0 | 19.3℃ | △H2 |
②△H1≠△H2原因是NaOH是强碱,NH3•H2O是弱碱电离吸热.

| A. | 有弱酸性,与Na2CO3、NaHCO3溶液均能反应 | |
| B. | 在一定条件下,1 mol该物质最多能与3 mol NaOH完全反应 | |
| C. | 在一定条件下,该物质可以发生取代、加成、水解、消去反应 | |
| D. | 该有机物分子中所有碳原子可能共平面 |
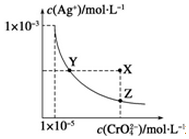 在t℃时,Ag2CrO4(橘红色)在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgBr的Ksp=5.0×10-13,下列说法错误的是( )
在t℃时,Ag2CrO4(橘红色)在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgBr的Ksp=5.0×10-13,下列说法错误的是( )| A. | t℃时,Ag2CrO4的Ksp为1×10-8 | |
| B. | 在饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点 | |
| C. | 一定温度下Y点和Z点时Ag2CrO4的Ksp相等 | |
| D. | 在t℃时,Ag2CrO4(s)+2Br-(aq)?2AgBr(s)+CrO42-(aq)平衡常数K=4.0×1010 |
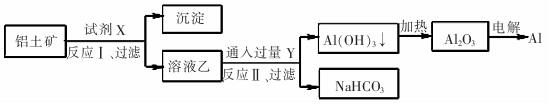
| A. | 试剂X为稀硫酸 | |
| B. | 反应Ⅱ中生成Al(OH)3的反应为:CO2+AlO2-+2H20=Al(OH)3↓+HCO3一 | |
| C. | 结合质子( H+)的能力由强到弱的顺序是Al02->CO32->OH- | |
| D. | Al2O3熔点很高,工业上还可采用电解熔融AICl3冶炼Al |
(1)在绝热固定容积的密闭容器发生反应:N2(g)+3H2(g)?2NH3(g),能说明上述反应向正反应方向移动的是②④
①单位时间内生成2n mol NH3的同时生成3n mol H2
②单位时间内生成6n mol N-H的同时生成2n mol H-H
③用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2
④混合气体的平均摩尔质量增大
⑤容器内气体密度不变
(2)已知合成氨反应在某温度下2L的密闭容器中进行,测得如下数据:
| 时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | 1.00 | 1.00 |
①反应进行到2小时时放出的热量为27.78KJ
②0~l小时内N2的平均反应速率0.05mol•L-1•h-1;
③此条件下该反应的化学平衡常数K=0.15(保留两位小数)
④反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1.00mol,化学平衡将向正反应方向移动(填“正反应”、“逆反应”或“不移动”).
 图示中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物,它们的焰色反应均为黄色.请填写下列空白:
图示中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物,它们的焰色反应均为黄色.请填写下列空白: 酸碱中和在化工生产中有着重要应用.
酸碱中和在化工生产中有着重要应用.