题目内容
2.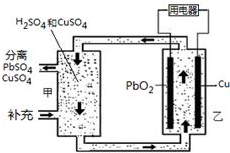 流动电池可以在电池外部调节电解质溶液,从而维持电池内部电解质溶液浓度稳定,原理如图.下列说法错误的是( )
流动电池可以在电池外部调节电解质溶液,从而维持电池内部电解质溶液浓度稳定,原理如图.下列说法错误的是( )| A. | Cu为负极 | |
| B. | PbO2电极的电极反应式为:PbO2+4H++SO42-+2e-=PbSO4+2H2O | |
| C. | 甲中应补充硫酸 | |
| D. | 当消耗1 mol PbO2,需分离出2 mol CuSO4 |
分析 根据电池总反应为Cu+PbO2+2H2SO4═CuSO4+PbSO4+2H2O,则铜失电子发生氧化反应为负极,反应式为:Cu-2e-═Cu2+,PbO2得电子发生还原反应为正极,反应式为:PbO2+4H++SO42-+2e-═PbSO4+2H2O,据此分析.
解答 解:A.根据电池总反应为Cu+PbO2+2H2SO4═CuSO4+PbSO4+2H2O,则铜失电子发生氧化反应为负极,故A正确;
B.PbO2得电子发生还原反应为正极,反应式为:PbO2+4H++SO42-+2e-═PbSO4+2H2O,故B正确;
C.由电池总反应为Cu+PbO2+2H2SO4═CuSO4+PbSO4+2H2O,则调节电解质溶液的方法是补充H2SO4,故C正确;
D.电池总反应为Cu+PbO2+2H2SO4═CuSO4+PbSO4+2H2O,当消耗1 mol PbO2,需分离出1mol CuSO4,故D错误;
故选D.
点评 本题考查了化学电源新型电池,根据原电池原理来分析解答,知道电极上发生的反应即可解答,电极反应式的书写是学习难点,总结归纳书写规律,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.甲、乙、丙、丁分别由H+、Na+、Al3+、Ba2+..OH-、Cl-、HCO3-离子中的两种组成的化合物,可以发生如图转化:下列说法错误的是( )
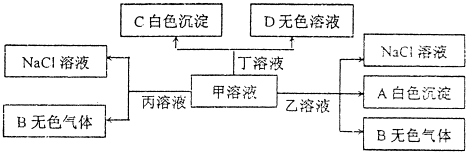

| A. | 乙为AlC13 | |
| B. | 能大量共存于溶液丙中的离子:Fe3+、SO42-、NO3- | |
| C. | 甲溶液中粒子的等量关系:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) | |
| D. | 甲溶液中滴加少量丁溶液反应的离子方程式:HCO3-+Ba2++OH-═BaCO3↓+H2O |
10.下列说法正确的是( )
| A. | 油脂是天然高分子化合物 | |
| B. | 蔗糖和麦芽糖互为同分异构体 | |
| C. | 蛋白质溶液中加入Na2SO4可使其变性 | |
| D. | 苯酚、甲醛通过加聚反应可制得酚醛树脂 |
17.下列有关化学与生活的说法错误的是( )
| A. | 铁粉、生石灰均可作食品抗氧化剂 | |
| B. | 明矾、氯化铁均可作净水剂 | |
| C. | 牛奶、鸡蛋清均可用于重金属中毒解毒 | |
| D. | 碘酒、双氧水均可用于伤口消毒 |
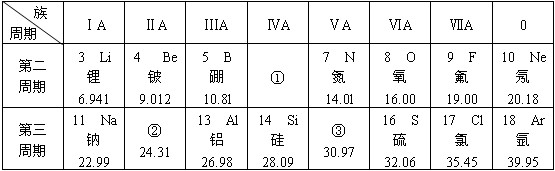
14.下列氢化物中最稳定的是( )
| A. | HF | B. | HCl | C. | HB | D. | HI |
11.利用CH4和CO2可以制造价值更高的化学产品.已知下列反应:
①CH4(g)+2O2(g)?CO2(g)+2H2O(g)△H1=akJ/mol
②CO(g)+H2O(g)?CO2(g)+H2(g)△H2=bkJ/mol
③2CO(g)+O2(g)?2CO2(g)△H3=ckJ/mol
(1)求反应CH4(g)+CO2(g)?2CO(g)+2H2(g)△H=a+2b-2c kJ/mol(用含a、b、c的代数式表示).
(2)一定条件下,等物质的量的(1)中反应生成的气体可合成二甲醚(CH3OCH3),同时还产生了一种可参与大气循环的无机化合物,该反应的化学方程式为3CO+3H2═CH3OCH3+CO2.
(3)用Cu2Al2O4做催化剂,一定条件下发生反应:
CO2(g)+CH4(g)?CH3COOH(g),温度与催化剂的催化效率和乙酸的生成速率的关系如图1所示,回答下列问题:
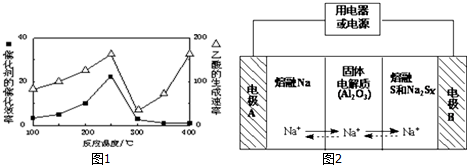
①250~300℃时,乙酸的生成速率降低的原因是催化剂的催化效率降低,化学反应速率降低.
②300~400℃时,乙酸的生成速率升高的原因是温度升高,化学反应速率加快.
(4)钠硫电池以熔融金属钠、熔融S和多硫化钠(Na2Sx)分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图2所示:Na2SX $?_{放电}^{充电}$2Na+xS (3<x<5)
①根据上表数据,请你判断该电池工作的适宜温度应控制在C范围内(填字母序号).
A.100℃以下 B.100℃~300℃C.300℃~350℃D.350~2050℃
(5)关于钠硫电池,下列说法正确的是AD(填字母序号).
A.放电时,电极A为负极
B.放电时,Na+的移动方向为从B到A
C.充电时,电极A应连接电源的正极
D.充电时电极B的电极反应式为SX2--2e-=xS
(6)25℃时,若用钠硫电池作为电源电解500mL0.2mol/LNaCl溶液,当溶液的pH变为l3时,电路中通过的电子的物质的量为0.05mol,两极的反应物的质量差为2.3g.(假设电解前两极的反应物的质量相等)
①CH4(g)+2O2(g)?CO2(g)+2H2O(g)△H1=akJ/mol
②CO(g)+H2O(g)?CO2(g)+H2(g)△H2=bkJ/mol
③2CO(g)+O2(g)?2CO2(g)△H3=ckJ/mol
(1)求反应CH4(g)+CO2(g)?2CO(g)+2H2(g)△H=a+2b-2c kJ/mol(用含a、b、c的代数式表示).
(2)一定条件下,等物质的量的(1)中反应生成的气体可合成二甲醚(CH3OCH3),同时还产生了一种可参与大气循环的无机化合物,该反应的化学方程式为3CO+3H2═CH3OCH3+CO2.
(3)用Cu2Al2O4做催化剂,一定条件下发生反应:
CO2(g)+CH4(g)?CH3COOH(g),温度与催化剂的催化效率和乙酸的生成速率的关系如图1所示,回答下列问题:

①250~300℃时,乙酸的生成速率降低的原因是催化剂的催化效率降低,化学反应速率降低.
②300~400℃时,乙酸的生成速率升高的原因是温度升高,化学反应速率加快.
(4)钠硫电池以熔融金属钠、熔融S和多硫化钠(Na2Sx)分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图2所示:Na2SX $?_{放电}^{充电}$2Na+xS (3<x<5)
| 物质 | Na | S | Al2O3 |
| 熔点/℃ | 97.8 | 115 | 2050 |
| 沸点/℃ | 892 | 444.6 | 2980 |
A.100℃以下 B.100℃~300℃C.300℃~350℃D.350~2050℃
(5)关于钠硫电池,下列说法正确的是AD(填字母序号).
A.放电时,电极A为负极
B.放电时,Na+的移动方向为从B到A
C.充电时,电极A应连接电源的正极
D.充电时电极B的电极反应式为SX2--2e-=xS
(6)25℃时,若用钠硫电池作为电源电解500mL0.2mol/LNaCl溶液,当溶液的pH变为l3时,电路中通过的电子的物质的量为0.05mol,两极的反应物的质量差为2.3g.(假设电解前两极的反应物的质量相等)
12.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 在水溶液中:H+、I-、NO3-、SiO32- | |
| B. | 饱和氯水中:Cl-、NO3-、Na+、SO32- | |
| C. | 碱性溶液中:NO3-、I-、Na+、Fe2+ | |
| D. | 将足量CO2通入时:H+、NH4+、Al3+、SO42- |
 .
.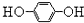 1,4一二羟基蒽醌结构简式
1,4一二羟基蒽醌结构简式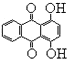
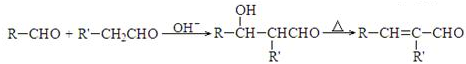
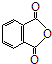 .
. .
.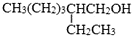 )反应可以制得另一种塑化剂DEHP.参照D的上述合成路线,设计一条由D为起始原料制备异辛醇的合成路线.
)反应可以制得另一种塑化剂DEHP.参照D的上述合成路线,设计一条由D为起始原料制备异辛醇的合成路线.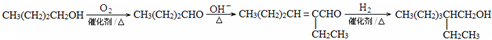 .
.