题目内容
下列物质:①盐酸 ②食盐水 ③熔化的氯化钠 ④液态氯化氢 ⑤铜 ⑥氨水 ⑦SO3 ⑧醋酸,其中可以导电并且属于强电解质的是( )
| A、只有③ | B、①②③⑥⑧ |
| C、④⑤ | D、全部都是 |
考点:强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:能导电的物质含有自由电子或自由离子,在水溶液里或熔融状态下能导电的化合物是电解质,能完全电离的电解质是强电解质,据此分析解答.
解答:
解:①盐酸、②食盐水、⑥氨水是混合物,所以不是电解质,但都含自由离子所以能导电,故错误.
③熔化氯化钠是强电解质且含有自由移动的离子所以能导电,故正确.
④液态氯化氢是强电解质,但没有自由移动的离子,所以不导电,故错误.
⑤铜是单质所以不是电解质,但能导电,故错误.
⑦三氧化硫是非电解质,不能导电,故错误.
⑧醋酸是弱电解质,没有自由离子所以不导电,故错误.
故选A.
③熔化氯化钠是强电解质且含有自由移动的离子所以能导电,故正确.
④液态氯化氢是强电解质,但没有自由移动的离子,所以不导电,故错误.
⑤铜是单质所以不是电解质,但能导电,故错误.
⑦三氧化硫是非电解质,不能导电,故错误.
⑧醋酸是弱电解质,没有自由离子所以不导电,故错误.
故选A.
点评:本题考查了能导电的强电解质的判断,难度不大,紧扣“强电解质、能导电”来分析解答即可.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
下列反应既属于化合反应又属于氧化还原反应的是( )
| A、SO2+H2O═H2SO3 | ||||
B、C+CO2
| ||||
C、H2+CuO
| ||||
D、CaCO3
|
据已有知识和元素性质递变规律来判断下列比较正确的是( )
| A、第二周期氢化物易燃性:CH4<NH3<H2O( ) |
| B、第三周期氢化物稳定性:SiH4>PH3>H2S>HCl |
| C、化合物毒性:若PH3>NH3,则H2S>H2O |
| D、氢化物的还原性:HF>H2O>NH3>CH4 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、使紫色石蕊试剂显红色的溶液:NH4+、K+、[Al(OH)4]-、NO3- |
| B、稀HNO3溶液:Na+、Mg2+、SO42-、Cl- |
| C、FeCl3溶液:K+、Na+、I-、SO42- |
| D、由水电离产生的c(H+)=10-13 mol?L-1的溶液:K+、Na+、Cl-、HCO3- |
X、Y、Z、W是原子序数依次增大的短周期主族元素,X、Z在周期表中的相对位置如下表.已知X元素最低负化合价的绝对值与其原子最外层电子数相等,Y是地壳中含量最多的金属元素.下列说法错误的是( )
| X | ||
| Z |
| A、X位于第二周期第ⅣA族 |
| B、原子半径由小到大的顺序为:W<Z<Y |
| C、Z、W两元素的气态氢化物中,Z的气态氢化物更稳定 |
| D、无论氧气是否过量,Z在氧气中燃烧的产物唯一 |
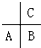 短周期元素A、B、C(均不为稀有气体元素)在周期表中的位置如图:下列说法正确的是( )
短周期元素A、B、C(均不为稀有气体元素)在周期表中的位置如图:下列说法正确的是( )| A、若均为非金属元素,其气态氢化物稳定性:A<B<C |
| B、若均为金属元素,其最高价氧化物的水化物的碱性:A<B<C |
| C、原子半径:A>C>B |
| D、最高正价:A>B>C |
除去粗盐中的Ca2+、Mg2+、SO42-,可将粗盐溶于水后进行如下操作:①过滤,②加过量的NaOH溶液,③加适量的盐酸,④加过量的Na2CO3溶液,⑤加过量的BaCl2溶液,⑥蒸发结晶,其中操作顺序正确的是( )
| A、①②③④⑤⑥ |
| B、②⑤④①③⑥ |
| C、①②④⑤③⑥ |
| D、④②③①⑤⑥ |
