题目内容
11.下列说法正确的是( )| A. | 原子的最外层电子数等于族序数 | |
| B. | 主族元素X、Y能形成XY3型化合物,序数差可能为2、6或8 | |
| C. | 分子结构相似的分子相对分子质量越大熔沸点越高 | |
| D. | 元素的原子得电子越多非金属性越强,失电子越多,金属性越强 |
分析 A.主族元素原子的最外层电子数等于该元素所在族序数,但副族元素不一定;
B.主族元素X、Y能形成XY3型化合物,可能有SO3、AlCl3、NH3等,据此判断;
C.如分子间存在氢键,则沸点较高;
D.金属性与失电子的多少无关.
解答 解:A.主族元素原子的最外层电子数等于该元素所在族序数,但副族元素不一定,故A错误;
B.主族元素X、Y能形成XY3型化合物,可能有SO3、AlCl3、NH3、PCl3,原子序数分别相差8、4和6和2,故B正确;
C.如分子间存在氢键,则沸点较高,如HF存在氢键,虽然HCl相对分子质量较大,但HF的沸点高,故C错误;
D.金属性强弱与失电子的多少无关,只与得失电子的难易程度有关,所以与最外层电子数无关,故D错误,故选B.
点评 本题考查较为综合,涉及氢键,元素周期律等知识,为高频考点,侧重于学生的分析能力和双基的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.下列反应的离子方程式正确的是( )
| A. | 大理石和硝酸:CO32-+2H+═H2O+CO2↑ | |
| B. | 铁和稀盐酸:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 稀硫酸和氨水:H++NH3•H2O═NH4++H2O | |
| D. | 碳酸氢钙溶液和盐酸:HCO3-+H+═H2O+CO2↑ |
2.以石墨电极电解200mL CuSO4溶液,电解过程中电子转移物质的量n(e-)与产生气体总体积V(g)(标准状况)的关系如图所示.下列说法中(忽略溶液体积变化)正确的是( )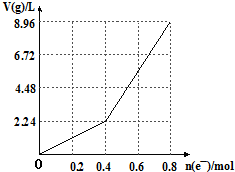

| A. | 电解前CuSO4溶液的物质的量浓度为2mol/L | |
| B. | 电解后所得溶液中c(H+)═2mol/L | |
| C. | 当n(e-)=0.6mol时,V(H2):V(O2)=3:2 | |
| D. | 向电解后的溶液中加入16gCuO,则溶液可恢复为电解前的浓度 |
6.除去NaNO3 溶液中混有的AgNO3,所用下列试剂中效果最好的是( )
| A. | NaCl 溶液 | B. | NaBr 溶液 | C. | NaI 溶液 | D. | Na2S 溶液 |
20.相同温度,相同物质的量浓度的五种溶液.按pH由大到小的顺序排列,正确的是( )
①NH4Cl ②NaHSO4 ③NaCl ④CH3COONa ⑤Na2CO3.
①NH4Cl ②NaHSO4 ③NaCl ④CH3COONa ⑤Na2CO3.
| A. | ⑤>④>①>③>② | B. | ⑤>④>③>①>② | C. | ⑤>④>①>②>③ | D. | ④>⑤>③>①>② |
1.下列说法正确的是( )
| A. | 将水加热,Kw增大,pH不变 | |
| B. | 燃烧热是指可燃物热化学反应方程式中的△H | |
| C. | 用25 mL碱式滴定管量取20.00mL高锰酸钾溶液 | |
| D. | 醋酸溶液的导电能力可能比稀硫酸强 |
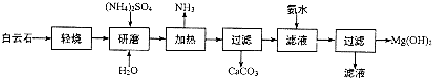
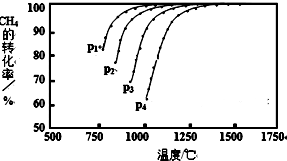
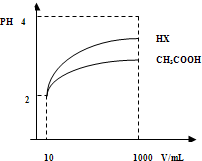 回答下列问题:
回答下列问题: