题目内容
 如图为实验室某盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
如图为实验室某盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制480mL物质的量浓度为0.400mol?L-1的稀盐酸.
①容量瓶上需标有以下五项中的
A.温度 B.浓度 C.容量 D.压强 E.刻度线
②将下列操作填写完整,并排列其正确的操作顺序(字母表示,每个字母只能用一次)
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取浓盐酸
C.将已冷却的盐酸沿玻璃杯注入
D.将容量瓶盖紧,颠倒摇匀
E.改用
F.继续往容量瓶内小心加水,直到液面接近刻度
③在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在横线上填“偏大”、“偏小”、无影响”).
Ⅰ用量筒量取浓盐酸时俯视观察凹液面
Ⅱ定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
Ⅲ定容时仰视刻度线
Ⅳ溶液注入容量瓶前没有回复到室温
考点:配制一定物质的量浓度的溶液
专题:实验题
分析:(1)根据c=
计算出该盐酸的物质的量浓度;
(2)根据各量的计算公式是否与溶液的体积有关判断;
(3)①根据容量瓶的构造及使用方法进行解答;
②根据配制一定物质的量浓度的溶液步骤对各操作进行排序;根据正确的配制方法进行解答;
③根据c=
可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量n和溶液的体积V引起的,误差分析时,关键要看配制过程中引起n和V怎样的变化:若n比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若n比理论值大,或V比理论值小时,都会使所配溶液浓度偏大.
| 1000ρw |
| M |
(2)根据各量的计算公式是否与溶液的体积有关判断;
(3)①根据容量瓶的构造及使用方法进行解答;
②根据配制一定物质的量浓度的溶液步骤对各操作进行排序;根据正确的配制方法进行解答;
③根据c=
| n |
| V |
解答:
解:(1)该浓盐酸的物质的量浓度为:c=
mol/L=11.9mol/L,
故答案为:11.9;
(2)A、n=c?V,所以溶液中HCl的物质的量与溶液体积有关,故A错误;
B、溶液的浓度是均一稳定的,与所取溶液的体积无关,故B正确;
C、N=n?NA=c?V?NA,所以与溶液体积有关,故C错误;
D、溶液的密度是均一的,所以与所取溶液的体积无关,故D正确;
故答案为:BD;
(3)①溶液体积受温度的影响,所以容量瓶上标有温度,容量瓶为 定量仪器,标有容量和刻度线,所以ACE正确,
故答案为:ACE;
②配制480mL物质的量浓度为0.400mol?L-1的稀盐酸,实验室没有480mL容量瓶,需要选用500mL容量瓶,实际上配制的是500mL 0.400mol/L的盐酸,配制的步骤为:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,所以正确的步骤为:BCAFED;
B.需要浓盐酸的体积为:
≈0.0168L=16.8mL;
C.已经冷却的溶液需要沿着玻璃棒转移到500mL容量瓶中;
E.最后定容时需要改用胶头滴管进行定容;
F.洗涤完烧杯和玻璃棒后,先直接加入蒸馏水直至距离容量瓶刻度线1-2cm时,改用胶头滴管定容,
故答案为:BCAFED;16.8;500mL容量瓶;胶头滴管;2~3cm;
③Ⅰ用量筒量取浓盐酸时俯视观察凹液面,导致量取的浓盐酸的体积偏小,配制的溶液浓度偏低,
故答案为:偏低;
Ⅱ定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水,导致配制的溶液体积偏大,配制的溶液浓度偏低,
故答案为:偏低;
Ⅲ定容时仰视刻度线,导致加入的蒸馏水超过了容量瓶刻度线,配制的溶液体积偏大,配制的溶液浓度偏低,
故答案为:偏低;
Ⅳ溶液注入容量瓶前没有回复到室温,热的溶液体积偏大,冷却后溶液体积变小,导致配制的溶液体积偏小,配制的溶液浓度偏高,
故答案为:偏高.
| 1000×1.19×36.5% |
| 36.5 |
故答案为:11.9;
(2)A、n=c?V,所以溶液中HCl的物质的量与溶液体积有关,故A错误;
B、溶液的浓度是均一稳定的,与所取溶液的体积无关,故B正确;
C、N=n?NA=c?V?NA,所以与溶液体积有关,故C错误;
D、溶液的密度是均一的,所以与所取溶液的体积无关,故D正确;
故答案为:BD;
(3)①溶液体积受温度的影响,所以容量瓶上标有温度,容量瓶为 定量仪器,标有容量和刻度线,所以ACE正确,
故答案为:ACE;
②配制480mL物质的量浓度为0.400mol?L-1的稀盐酸,实验室没有480mL容量瓶,需要选用500mL容量瓶,实际上配制的是500mL 0.400mol/L的盐酸,配制的步骤为:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,所以正确的步骤为:BCAFED;
B.需要浓盐酸的体积为:
| 0.400mol/L×0.5L |
| 11.9mol/L |
C.已经冷却的溶液需要沿着玻璃棒转移到500mL容量瓶中;
E.最后定容时需要改用胶头滴管进行定容;
F.洗涤完烧杯和玻璃棒后,先直接加入蒸馏水直至距离容量瓶刻度线1-2cm时,改用胶头滴管定容,
故答案为:BCAFED;16.8;500mL容量瓶;胶头滴管;2~3cm;
③Ⅰ用量筒量取浓盐酸时俯视观察凹液面,导致量取的浓盐酸的体积偏小,配制的溶液浓度偏低,
故答案为:偏低;
Ⅱ定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水,导致配制的溶液体积偏大,配制的溶液浓度偏低,
故答案为:偏低;
Ⅲ定容时仰视刻度线,导致加入的蒸馏水超过了容量瓶刻度线,配制的溶液体积偏大,配制的溶液浓度偏低,
故答案为:偏低;
Ⅳ溶液注入容量瓶前没有回复到室温,热的溶液体积偏大,冷却后溶液体积变小,导致配制的溶液体积偏小,配制的溶液浓度偏高,
故答案为:偏高.
点评:本题考查了配制一定物质的量浓度的溶液的方法,题目难度中等,试题涉及的题量较大,侧重对学生能力的培养和解题方法的指导和训练,有利于培养学生的逻辑思维能力和严谨的规范实验操作能力;该题的难点在于误差分析,注意明确误差分析的方法与技巧.

练习册系列答案
相关题目
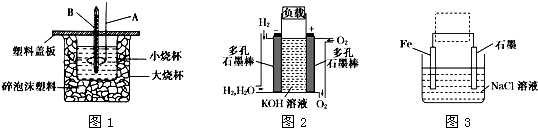
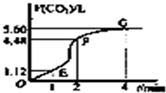 向200mL 6mol/L的盐酸中加入一定量的纯净CaCO3,产生气体的体积随时间的变化曲线如图所示(气体体积均在标准状况下测定).请回答下列问题:
向200mL 6mol/L的盐酸中加入一定量的纯净CaCO3,产生气体的体积随时间的变化曲线如图所示(气体体积均在标准状况下测定).请回答下列问题: 某课外活动小组同学用右下图装置进行以下表格中的三组实验,两极各有一个盛满水倒扣的小试管用来收集气体,W为浸有饱和硫酸钠和酚酞混合溶液的滤纸片,试回答下列问题:
某课外活动小组同学用右下图装置进行以下表格中的三组实验,两极各有一个盛满水倒扣的小试管用来收集气体,W为浸有饱和硫酸钠和酚酞混合溶液的滤纸片,试回答下列问题: