题目内容
17.同周期的X、Y、Z三种元素,已知其最高价氧化物对应水化物的酸性:H3XO4<H2YO4<HZO4.下列判断正确的是( )| A. | 非金属性:X>Y>Z | B. | 气态氢化物的稳定性:X>Y>Z | ||
| C. | 原子半径:X<Y<Z | D. | 对应阴离子的还原性:X>Y>Z |
分析 同周期的X、Y、Z三种元素,已知其最高价氧化物对应水化物的酸性:H3XO4<H2YO4<HZO4,则非金属性X<Y<Z,结合同周期元素性质来解答.
解答 解:A.由同周期元素的最高价氧化物对应水化物的酸性:H3XO4<H2YO4<HZO4,非金属性X<Y<Z,故A错误;
B.非金属性X<Y<Z,则气态氢化物的稳定性为X<Y<Z,故B错误;
C.同周期从左向右非金属性增强,原子半径减小,则原子半径为X>Y>Z,故C错误;
D.非金属性X<Y<Z,则对应阴离子的还原性:X>Y>Z,故D正确;
故选D.
点评 本题考查原子结构与元素周期律,为高频考点,把握非金属性的比较、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
8.乙烷在光照的条件下与氯气混和,共可以生成几种物质( )
| A. | 7种 | B. | 8种 | C. | 9种 | D. | 10种 |
5.NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 12g金刚石中含σ键数为4 NA | |
| B. | 1mol Na2O2固体中含离子总数为4 NA | |
| C. | ag C2H4和C3H6的混合物所含碳氢键数目为$\frac{a{N}_{A}}{14}$ | |
| D. | 30g甲醛中含π键数为NA |
2.下列关于卤素的说法正确的是( )
| A. | Cl2能与水反应,在反应中Cl2只能作氧化剂 | |
| B. | 氧化性Cl2>Br2>I2,还原性Cl->Br->I- | |
| C. | 实验室制备Cl2,可用排饱和食盐水集气法收集 | |
| D. | 氯水具有酸性,可用pH试纸测量其pH值 |
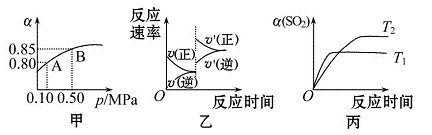
 2SO3(g) ΔH<0.某温度下,将2 mol SO2和1 mol O2置于 10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与
2SO3(g) ΔH<0.某温度下,将2 mol SO2和1 mol O2置于 10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与 体系总压强(p)的关系如图甲所示。则下列说法正确的是( )
体系总压强(p)的关系如图甲所示。则下列说法正确的是( )