题目内容
9.下列事实不能用元素周期律解释的是( )| A. | 热稳定性:Na2CO3>NaHCO3 | B. | 酸性:H2CO3>H2SiO3 | ||
| C. | 碱性:NaOH>LiOH | D. | 热稳定性:HF>HBr |
分析 A.碳酸氢盐易分解,碳酸盐难分解;
B.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
C.元素的金属性越强,对应的最高价氧化物的水化物的碱性越强;
D.元素的非金属性越强,气态氢化物的稳定性越强.
解答 解:A.碳酸氢盐易分解,碳酸盐难分解,所以热稳定性:Na2CO3>NaHCO3,不能用元素周期律解释,故A选;
B.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,非金属性:C>Si,则酸性:H2CO3>H2SiO3,能用元素周期律解释,故B不选;
C.元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,金属性:Na>Li,则碱性:NaOH>LiOH,能用元素周期律解释,故C不选;
D.元素的非金属性越强,气态氢化物的稳定性越强,非金属性:F>Br,热稳定性:HF>HBr,故D不选.
故选A.
点评 本题考查了元素周期律的理解与应用,注意把握元素周期律的递变规律以及相关知识的积累,难度不大.

练习册系列答案
相关题目
16.某乙酸乙酯(CH3C18OOCH2CH3),它在酸性水中充分水解后,可以检测到含有18O的分子是( )
| A. | 乙酸 | B. | 乙醇 | C. | 水 | D. | 乙酸乙酯 |
14.化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法错误的是( )
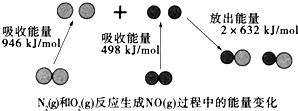

| A. | 该反应的热化学方程式为:N2(g)+O2(g)═2NO(g)△H=+180kJ•mol-1 | |
| B. | 1mol N2(l)和NA个O2(l)反应生成2mol NO(g)时,吸收的能量为180kJ | |
| C. | 1mol N2(g)和1mol O2(g)具有的总能量小于2mol NO(g)具有的总能量 | |
| D. | 通常情况下,N2(g)和O2(g)混合不能直接生成NO(g) |
1.研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发生反应2NO(g)+O2(g)?2NO2(g),下列各项能说明反应达到平衡状态的是abc.
a.体系压强保持不变
b.混合气体颜色保持不变
c.NO和O2的物质的量之比保持不变
d.每消耗1molO2同时生成2molNO2
(2)CO可用于合成甲醇,一定温度下,向体积为2L的密闭容器中加入CO和H2,发生反应CO(g)+2H2(g)?CH3OH(g),达平衡后测得各组分浓度如下:
①列式并计算平衡常数K=$\frac{2}{3}$.
②若降低温度,K值增大,则反应的△H<0(填“>”或“<”).
③若保持体积不变,再充入0.6molCO和0.4molCH3OH,此时v正=v逆(填“>”、“<”或“=”)
(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发生反应2NO(g)+O2(g)?2NO2(g),下列各项能说明反应达到平衡状态的是abc.
a.体系压强保持不变
b.混合气体颜色保持不变
c.NO和O2的物质的量之比保持不变
d.每消耗1molO2同时生成2molNO2
(2)CO可用于合成甲醇,一定温度下,向体积为2L的密闭容器中加入CO和H2,发生反应CO(g)+2H2(g)?CH3OH(g),达平衡后测得各组分浓度如下:
| 物质 | CO | H2 | CH3OH |
| 浓度(mol•L-1) | 0.9 | 1.0 | 0.6 |
②若降低温度,K值增大,则反应的△H<0(填“>”或“<”).
③若保持体积不变,再充入0.6molCO和0.4molCH3OH,此时v正=v逆(填“>”、“<”或“=”)
19.已知aR2+微粒核外有b个电子,则N克该微粒所含的中子数为( )
| A. | a-b+2 | B. | $\frac{N(a-b-2)}{a}$ | C. | $\frac{N(a-b+2)}{a}$ | D. | a-b-2 |
 .
.