题目内容
8. 重铬酸钾(K2Cr2O7)是一种重要的氧化剂,可以检验司机是否酒后驾驶.
重铬酸钾(K2Cr2O7)是一种重要的氧化剂,可以检验司机是否酒后驾驶.2Cr2O72-+3CH3CH2OH+16H++13H2O→4[Cr(H2O)6]3++3CH3COOH
(1)铬原子核外有6个未成对电子,Cr3+基态核外电子排布式为1s22s22p63s23p63d3.
(2)CH3COOH中C原子轨道杂化类型为sp3杂化、sp2杂化.
(3)CH3CH2OH与H2O可以任意比例互溶,是因为H2O与乙醇分子间形成氢键,都为极性分子.
(4)C、O位于周期表中第二周期,请比较两者第一电离能大小:C<O(填“<”或“>”)
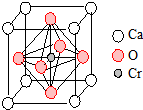
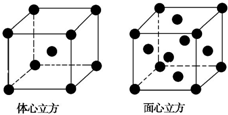
(5)Cr和Ca可以形成一种具有特殊导电性的复合氧化物,晶胞如图所示.该晶体的化学式为CaCrO3.
分析 (1)铬原子核外有24个电子,核外电子排布为1s22s22p63s23p63d54s1,据此判断未成对电子;Cr原子失去最外层1个电子和3d轨道上的2个电子形成Cr3+;
(2)CH3COOH中C原子分别形成4个、3个δ键,没有孤对电子;
(3)H2O与CH3CH3OH都含有氢键,且都为极性分子;
(4)同一周期元素的第一电离能随着原子序数增大而增大,但第IIA族、第VA族元素第一电离能大于其相邻元素;
(5)利用均摊法计算该物质的化学式.
解答 解:(1)铬原子核外有24个电子,核外电子排布为1s22s22p63s23p63d54s1,所以未成对的电子数目为6个;Cr原子失去最外层1个电子和3d轨道上的2个电子形成Cr3+,该离子核外电子排布式为:1s22s22p63s23p63d3;
故答案为:6;1s22s22p63s23p63d3;
(2)CH3COOH中C原子分别形成4个、3个δ键,没有孤对电子,分别为sp3杂化、sp2杂化;
故答案为:sp3杂化、sp2杂化;
(3)H2O与CH3CH2OH都含有氢键,且都为极性分子,二者任意比例互溶;
故答案为:H2O与乙醇分子间形成氢键,都为极性分子;
(4)C、O元素处于同一周期且原子序数逐渐增大,所以第一电离能大小为:O>C;
故答案为:<;
(5)根据晶胞结构图和均摊法可知,晶胞中O原子数为$\frac{1}{2}$×6=3,Ca原子数为$\frac{1}{8}$×8=1,Cr原子数为1,则化学式为CaCrO3;
故答案为:CaCrO3.
点评 本题考查较为综合,题目难度较大,涉及第一电离能的判断、电子排布式、杂化类型的判断、晶胞的计算等,注意利用均摊法计算晶胞的构成.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.设NA为阿伏加德罗常数的数值.则下列说怯中正确的是
①2.24L氨气含有NA个电子
②1.4g乙烯与丙烯的混合气体含有NA个碳原子
③精炼铜,若阳极失去2NA个电予.则阴极增重64g
④标准状况下,22.4L空气含有NA个分子
⑤过氧化钠与水反应.若电子转移2NA,则产生的氧气为32g
⑥将IL2mol/L的FeCl3溶液加人到沸水中.加热使之完全反应.所得氢氧化铁子数为2NA
⑦在1L0.1mol/L的碳酸钠溶液中.阴离子总数大于0.1NAA.
①2.24L氨气含有NA个电子
②1.4g乙烯与丙烯的混合气体含有NA个碳原子
③精炼铜,若阳极失去2NA个电予.则阴极增重64g
④标准状况下,22.4L空气含有NA个分子
⑤过氧化钠与水反应.若电子转移2NA,则产生的氧气为32g
⑥将IL2mol/L的FeCl3溶液加人到沸水中.加热使之完全反应.所得氢氧化铁子数为2NA
⑦在1L0.1mol/L的碳酸钠溶液中.阴离子总数大于0.1NAA.
| A. | ③④⑤⑦ | B. | ①③④⑦ | C. | ②③④⑤⑦ | D. | ②④⑤⑦ |
16.下列说法中不正确的是( )
| A. | 元素周期表,一共18个纵行,而元素种类最多的族,在第3纵行 | |
| B. | 无论是吸热反应还是放热反应,升高温度,都能使反应速率加快 | |
| C. | 假设石墨转化为金刚石,需要吸收能量,则说明石墨比金刚石更稳定 | |
| D. | 非金属元素的非金属性越强,其氧化物对应的水化物酸性也一定越强 |
13.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 2.8g铁粉在1.12L(标准状况下)氯气中充分燃烧,失去的电子数为0.15NA | |
| B. | 标准状况下22.4LSO3含氧原子数为3NA | |
| C. | 10g H218O中所含的中子数为5NA | |
| D. | 11.2L 的CO气体与0.5molN2所含的电子数相等 |
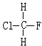 与
与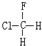 B.
B.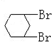 与
与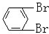 C.
C.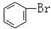 与
与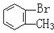 D.
D.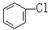 与
与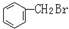 E.ClC(CH3)3与(CH3)2CHCH2Cl F.
E.ClC(CH3)3与(CH3)2CHCH2Cl F.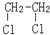 与CH3-CH2Cl.
与CH3-CH2Cl.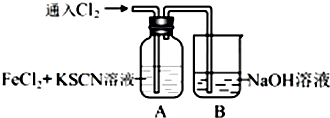
 ,偏碱性条件下,氰化钠溶液的CN-被双氧水氧化为HCO3-,同时放出NH3,该反应的离子方程式为CN-+H2O2+H2O═NH3↑+HCO3-.
,偏碱性条件下,氰化钠溶液的CN-被双氧水氧化为HCO3-,同时放出NH3,该反应的离子方程式为CN-+H2O2+H2O═NH3↑+HCO3-.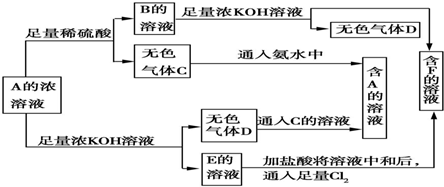
 氮族元素是指位于元素周期表第15列的元素,包括氮、磷、砷(As)、锑(Sb)、铋(Bi)五种元素.请回答下列问题:
氮族元素是指位于元素周期表第15列的元素,包括氮、磷、砷(As)、锑(Sb)、铋(Bi)五种元素.请回答下列问题: