题目内容
19.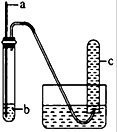 用如图装置进行实验,下列预期实验现象及相应结论均正确的是( )
用如图装置进行实验,下列预期实验现象及相应结论均正确的是( )| a | b | 预期实验 现象 | 结论 | |
| A | 铜丝 | 浓硝酸 | 试管c中有大量红棕色气体 | 硝酸有强氧化性 |
| B | 木条 | 18.4mol/L 硫酸 | 木条变黑 | 浓硫酸有酸性及 氧化性 |
| C | 生铁 | NaCl溶液 | 导管处发生倒吸 | 生铁发生吸氧腐蚀 |
| D | 铁丝 | 含少量HCl的H2O2溶液 | 试管c中有大量无色气体 | 该反应中铁作催化剂 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Cu和浓硝酸反应生成红棕色气体二氧化氮,但二氧化氮能和水反应生成硝酸和NO;
B.浓硫酸具有脱水性,能将H、O元素以2:1水的形式脱去而体现脱水性;
C.酸性条件下,生铁发生析氢腐蚀,在中性或弱酸性条件下生铁发生吸氧腐蚀;
D.铁和HCl反应生成氯化亚铁和氢气,双氧水分解生成水和氧气.
解答 解:A.Cu和浓硝酸反应生成红棕色气体二氧化氮,但二氧化氮能和水反应生成硝酸和NO,所以试管c中得不到红棕色气体,故A错误;
B.浓硫酸将木条中的H、O元素以2:1水的形式脱去而体现脱水性,能使木条变黑体现脱水性和强氧化性,故B错误;
C.酸性条件下,生铁发生析氢腐蚀,在中性或弱酸性条件下生铁发生吸氧腐蚀,所以在NaCl溶液中能发生吸氧腐蚀,b中压强减小,导致导管处发生倒吸,故C正确;
D.铁和HCl反应生成氯化亚铁和氢气,双氧水分解生成水和氧气,所以该实验中Fe不做催化剂,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及气体的收集、金属的腐蚀与防护、浓硫酸的性质等知识点,明确实验原理、物质性质是解本题关键,注意实验操作规范性、实验原理及实验评价,题目难度不大.

练习册系列答案
 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
10.下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 25℃时,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12溶液.Na+、SO32一、ClO-、CO32- | |
| B. | 能与金属铝反应放出氢气的溶液中:K+、Fe2+、Cl-、NO3- | |
| C. | 0.1mol/LBa (OH)2溶液中:Al3+、NH4+、NO3-、HCO3- | |
| D. | 0.1mol/L AlO2-溶液中:Na+、K+、SO32一、CO32- |
11.下列有关化学实验操作、现象或结论的描述正确的是( )
| A. | 乙烯通入溴水中,测定反应前后溶液pH,pH增大,乙烯与溴发生取代反应 | |
| B. | 向某溶液中加入KSCN溶液和稀盐酸,溶液变红色,原溶液一定有Fe3+ | |
| C. | 将湿润的氨气通过无水CaCl2,可得到干燥的氨气 | |
| D. | 分别取一块小木条,放入饱和硅酸钠溶液和蒸馏水中,充分吸湿、浸透,取出稍沥干后,置于酒精灯外焰处,前者木条未燃烧,后者燃烧,可证明硅酸钠可作木材防火剂 |
8.乙烯的结构简式为CH2=CH2,含有不饱和的C=C双键,能使KMnO4溶液和溴的溶液褪色,但不能发生( )
| A. | 氧化反应 | B. | 加成反应 | C. | 加聚反应 | D. | 酯化反应 |
9.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1mol/LNaCl溶液含有NA个Na+ | |
| B. | 任意条件下,16gO3所含的原子数为NA | |
| C. | 1molFe与足量稀HNO3反应,转移3NA个电子 | |
| D. | 标准状况下,22.4LSO3所含的分子数为NA |
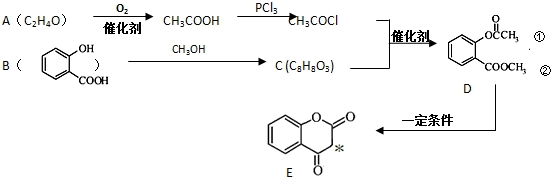
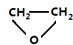 .
.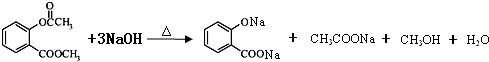 .
.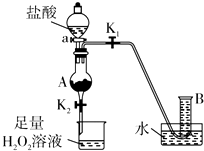 氯化铁是实验室中的重要试剂.某同学用m g含有铁锈(Fe2O3)的废铁屑来制取FeCl3•6H2O晶体,同时测定废铁屑中铁的质量分数,为此设计了如图装置(夹持装置略,气密性已检验):
氯化铁是实验室中的重要试剂.某同学用m g含有铁锈(Fe2O3)的废铁屑来制取FeCl3•6H2O晶体,同时测定废铁屑中铁的质量分数,为此设计了如图装置(夹持装置略,气密性已检验):