题目内容
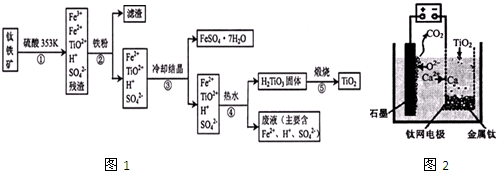
工业上,以钛铁矿为原料制备二氧化钛的某工艺流程如图1所示.钛铁矿主要成分为钛酸亚铁( TETiO3).其中一部分铁元素在风化过程中会转化为+3价.
完成下列填空:
(1)步骤②中,用铁粉将Fe3+转化为Fe2+的反应的离子方程式为 .
(2)步骤③中,实现混合物的分离是利用物质的 (填字母序号).
a.熔沸点差异 b溶解性差异 c氧化性、还原性差异
(3)步骤②、③、④中,均需进行的操作是 (填操作名称).
(4)可利用生产过程中的废液与软锰矿(主要成分MnO2)反应生产硫酸锰,则反应的离子方程式为
(5)利用图2装置,石墨作阳极,钛网作阴极,熔融CaF2-CaO做电解质,可获得金属钙,钙再作为还
原剂,可还原二氧化钛制各金属钛.
①阳极所发生的反应为 .
②在制备金属钛前后,CaO的总量不变,其原因是 .
(6)T业上用4.0吨钛铁矿制得1 6吨的二氧化钛,则钛铁矿中钛元素的质量分数是 .(假设生产过程中钛没有损失)

完成下列填空:
(1)步骤②中,用铁粉将Fe3+转化为Fe2+的反应的离子方程式为
(2)步骤③中,实现混合物的分离是利用物质的
a.熔沸点差异 b溶解性差异 c氧化性、还原性差异
(3)步骤②、③、④中,均需进行的操作是
(4)可利用生产过程中的废液与软锰矿(主要成分MnO2)反应生产硫酸锰,则反应的离子方程式为
(5)利用图2装置,石墨作阳极,钛网作阴极,熔融CaF2-CaO做电解质,可获得金属钙,钙再作为还
原剂,可还原二氧化钛制各金属钛.
①阳极所发生的反应为
②在制备金属钛前后,CaO的总量不变,其原因是
(6)T业上用4.0吨钛铁矿制得1 6吨的二氧化钛,则钛铁矿中钛元素的质量分数是
考点:物质分离和提纯的方法和基本操作综合应用,电解原理
专题:实验设计题,电化学专题
分析:(1)金属铁可以和铁离子反应生成亚铁离子,结合电荷守恒、原子守恒配平写出离子方程式;
(2)根据物质溶解度本题分析析出晶体的条件应用;
(3)依据操作过程中形成的物质溶解性和分离目的分析回答;
(4)依据二氧化锰的氧化性氧化亚铁离子分析氧化还原反应生成二价锰的化合物,结合电荷守恒和原子守恒写出;
(5)①依据图示生成物质的分析,阳极生成二氧化碳,阴极析出钙,结合电解池中阳极发生氧化反应,阴极发生还原反应,写出电极反应;
②根据电解槽中发生的反应:2CaO
2Ca+O2↑以及钙还原二氧化钛反应方程式:2Ca+TiO2=Ti+2CaO来回答;
(6)根据钛原子守恒进行解答.
(2)根据物质溶解度本题分析析出晶体的条件应用;
(3)依据操作过程中形成的物质溶解性和分离目的分析回答;
(4)依据二氧化锰的氧化性氧化亚铁离子分析氧化还原反应生成二价锰的化合物,结合电荷守恒和原子守恒写出;
(5)①依据图示生成物质的分析,阳极生成二氧化碳,阴极析出钙,结合电解池中阳极发生氧化反应,阴极发生还原反应,写出电极反应;
②根据电解槽中发生的反应:2CaO
| ||
(6)根据钛原子守恒进行解答.
解答:
解:(1)用铁粉将Fe3+转化为Fe2+的反应的离子方程式为:2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+;
(2)步骤③冷却结晶得到硫酸亚铁晶体,利用的是物质溶解度的不同,通过冷却热饱和溶液得到,故答案为:b;
(3)②③④步骤的操作过程中都得到沉淀或晶体,所以需要过滤得到固体和溶液,故答案为:过滤;
(4)利用生产过程中的废液与软锰矿(主要成分为MnO2)反应生产硫酸锰(MnSO4,易溶于水),利用二氧化锰的氧化性氧化亚铁离子为三价铁离子,反应的离子方程式为MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,故答案为:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
(5)①用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,阳极发生氧化反应,阴极析出钙金属发生还原反应,阳极图示产物可可知,阳极生成二氧化碳气体,是电解质中的氧离子失电子生成氧气,氧气和阳极石墨反应生成的二氧化碳,所以电极反应为:2O2--4e-=O2↑,或C+2O2--4e-=CO2↑;
故答案为:2O2--4e-=O2↑,或C+2O2--4e-=CO2↑;
②阴极上电极反应式为:2Ca2++4e-═2Ca,阳极上电极反应为:2O2--4e-=O2↑,电解槽中发生反应:2CaO
2Ca+O2↑,钙还原二氧化钛反应方程式为:2Ca+TiO2=Ti+2CaO,在制备金属钛前后,整套装置中CaO的总量不变,故答案为:电解槽中发生反应:2CaO
2Ca+O2↑,钙还原二氧化钛反应方程式为:2Ca+TiO2=Ti+2CaO,在制备金属钛前后,整套装置中CaO的总量不变;
(6)如果取钛铁矿4t,生产出16吨的二氧化钛,其中钛元素的质量是16×
×100%=9.6t,所以钛铁矿中钛的质量分数
×100%=24%,
故答案为:24%.
(2)步骤③冷却结晶得到硫酸亚铁晶体,利用的是物质溶解度的不同,通过冷却热饱和溶液得到,故答案为:b;
(3)②③④步骤的操作过程中都得到沉淀或晶体,所以需要过滤得到固体和溶液,故答案为:过滤;
(4)利用生产过程中的废液与软锰矿(主要成分为MnO2)反应生产硫酸锰(MnSO4,易溶于水),利用二氧化锰的氧化性氧化亚铁离子为三价铁离子,反应的离子方程式为MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,故答案为:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
(5)①用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,阳极发生氧化反应,阴极析出钙金属发生还原反应,阳极图示产物可可知,阳极生成二氧化碳气体,是电解质中的氧离子失电子生成氧气,氧气和阳极石墨反应生成的二氧化碳,所以电极反应为:2O2--4e-=O2↑,或C+2O2--4e-=CO2↑;
故答案为:2O2--4e-=O2↑,或C+2O2--4e-=CO2↑;
②阴极上电极反应式为:2Ca2++4e-═2Ca,阳极上电极反应为:2O2--4e-=O2↑,电解槽中发生反应:2CaO
| ||
| ||
(6)如果取钛铁矿4t,生产出16吨的二氧化钛,其中钛元素的质量是16×
| 48 |
| 80 |
| 9.6 |
| 4 |
故答案为:24%.
点评:本题考查了物质分离的流程分析判断,物质性质的应用,离子性质的应用,分离操作的方法,氧化还原反应的离子方程式的书写方法,电解池原理的应用,电极反应的书写原则.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数,下列判断正确的是( )
| A、常温常压下,16g O2和O3的混合气体中含有NA个氧原子 |
| B、常温常压下,28 g CO与22.4 L O2的分子数都是NA个 |
| C、16 g CH4与18 g NH4+所含质子数都是10NA个 |
| D、1 mol/L Na2CO3溶液中,CO32-的离子数目小于NA个 |
下列实验设计能完成或实验结论合理的是( )
| A、证明一瓶红棕色气体是溴蒸气还是二氧化氮,可用湿润的碘化钾--淀粉试纸检验,观察试纸颜色的变化 |
| B、铝热剂溶于足量稀盐酸再滴加KSCN溶液,未出现血红色,铝热剂中一定不含铁的氧化物 |
| C、将SO2通入Ba(NO3)2溶液,有白色沉淀生成,证明BaSO3难溶于硝酸 |
| D、在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,验证Na2CO3溶液中存在水解平衡 |
以下元素基态原子电子排布图正确的是( )
A、 |
B、 |
C、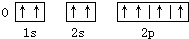 |
D、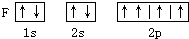 |
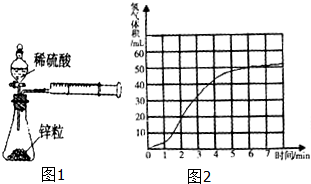 某课题组研究锌与稀硫酸的反应速率及影响因素,实验装置如图1所示.
某课题组研究锌与稀硫酸的反应速率及影响因素,实验装置如图1所示.