题目内容
若溶液中由水电离产生的c(OH-)=1×10-14mol?L-1,满足此条件的溶液中一定能大量共存的离子组是( )
| A、Al3+ Na+ NO3- Cl- |
| B、K+ Na+ Cl- NO3- |
| C、K+ Na+ Cl- HCO3- |
| D、K+ Fe2+ SO42- NO3- |
考点:离子共存问题
专题:离子反应专题
分析:若溶液中由水电离产生的c(OH-)=1×10-14mol?L-1<10-7mol?L-1,说明该溶液呈酸性或碱性,如果能共存,则这几种离子和氢离子或氢氧根离子之间不反应,据此分析解答.
解答:
解:若溶液中由水电离产生的c(OH-)=1×10-14mol?L-1<10-7mol?L-1,说明该溶液呈酸性或碱性,
A.这几种离子之间不反应,但碱性条件下Al3+不能存在,故A错误;
B.这几种离子之间不反应,且这几种离子和氢离子或氢氧根离子都不反应,所以满足此条件的溶液中一定能大量共存,故B正确;
C.HCO3-在酸性或碱性溶液中都不能大量存在,故C错误;
D.酸性条件下,Fe2+和NO3-发生氧化还原反应而不能共存,故D错误;
故选B.
A.这几种离子之间不反应,但碱性条件下Al3+不能存在,故A错误;
B.这几种离子之间不反应,且这几种离子和氢离子或氢氧根离子都不反应,所以满足此条件的溶液中一定能大量共存,故B正确;
C.HCO3-在酸性或碱性溶液中都不能大量存在,故C错误;
D.酸性条件下,Fe2+和NO3-发生氧化还原反应而不能共存,故D错误;
故选B.
点评:本题考查了离子共存,根据水的电离程度确定溶液酸碱性,再结合离子共存条件来分析解答,易错选项是D,注意:酸性条件下亚铁离子和硝酸根离子能发生反应3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
有下列物质:①8.5gNH3 ②标准状况下22.4LH2 ③4℃时10mlH2O ④0.2molH3PO4按所含的分子数由多到少的顺序排列正确的是( )
| A、①④③② | B、④③②① |
| C、②③①④ | D、①②③④ |
下列处理不正确的是( )
| A、小苏打沾在手上立即用水冲洗 |
| B、用试管或烧杯给液体加热时,均没有垫石棉网 |
| C、为防止新鲜肉类变质,用食盐溶液浸泡保鲜 |
| D、做实验时,皮肤上沾了浓硫酸立即用干布拭去并用大量水冲洗 |
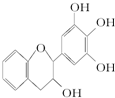 茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中不正确的是( )
茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中不正确的是( )| A、EGC分子式为C15H12O5 |
| B、1 mol EGC与3 mol NaOH恰好完全反应 |
| C、易发生氧化反应和取代反应,能发生加成反应 |
| D、遇FeCl3溶液发生显色反应 |
在容积不变的密闭容器中存在反应:2A(g)+B(g)
2C(g)△H<0;某研究小组研究了只改变某一反应条件对上述反应的影响,下列说法正确的是( )
| 催化剂 |
| 加热 |

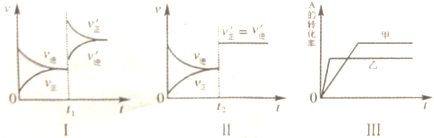
| A、图Ⅰ表示的是t1时刻增大B的浓度对反应速率的影响 |
| B、图Ⅱ表示的是t2时刻加入催化剂后对反应速率的影响 |
| C、图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙高 |
| D、图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高 |
相同状况下,下列气体所占体积最大的是( )
| A、32g SO2 |
| B、32g O2 |
| C、73gHCl |
| D、5g H2 |
1mol某有机物在稀硫酸作用下,水解生成2mol相同的物质.下列物质中,符合题意的物质可能是( )
①蔗糖 ②麦芽糖 ③淀粉
④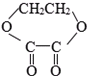 ⑤
⑤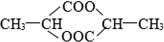 ⑥
⑥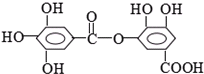
①蔗糖 ②麦芽糖 ③淀粉
④
 ⑤
⑤ ⑥
⑥
| A、①②⑤ | B、④⑤ |
| C、①⑤⑥ | D、②⑤⑥ |
下列物质只有在水溶液中能导电,且属于电解质的是( )
| A、食盐 | B、酒精 | C、乙酸 | D、氨气 |