题目内容
在25℃时,用蒸馏水稀释1mol/L的醋酸溶液至0.01mol/L,随溶液的稀释,下列说法正确的是( )
| A、溶液中所有离子浓度均减小 | ||
| B、pH的变化值等于2 | ||
C、溶液中
| ||
| D、分别与足量的Mg粉反应,0.01 mol/L的醋酸溶液产生的氢气较少 |
考点:弱电解质在水溶液中的电离平衡
专题:
分析:加水稀释,促进醋酸的电离,n(CH3COO-)、n(H+)增大,但浓度减小,以此解答即可.
解答:
解:A、加水稀释醋酸,其溶液中氢氧根离子浓度增大,故A错误;
B、用蒸馏水稀释1mol/L的醋酸溶液至0.01mol/L,加水稀释,促进醋酸的电离,则pH变化小于2,故B错误;
C、加水稀释醋酸,其溶液中氢离子、醋酸浓度均减小,但是氢离子浓度减小的程度小,所以溶液中
保持增大趋势,故C正确;
D、分别与足量的Mg粉反应,0.01mol/L的醋酸溶液中的氢离子量少,所以0.1mol/L的醋酸产生的氢气多,故D错误.
故选C.
B、用蒸馏水稀释1mol/L的醋酸溶液至0.01mol/L,加水稀释,促进醋酸的电离,则pH变化小于2,故B错误;
C、加水稀释醋酸,其溶液中氢离子、醋酸浓度均减小,但是氢离子浓度减小的程度小,所以溶液中
| c(H+) |
| c(CH3COOH) |
D、分别与足量的Mg粉反应,0.01mol/L的醋酸溶液中的氢离子量少,所以0.1mol/L的醋酸产生的氢气多,故D错误.
故选C.
点评:本题综合考查醋酸的电离,注意加水稀释醋酸,能促进醋酸电离,但溶液中醋酸根离子增大的量远远小于水体积增大的量,所以醋酸根离子浓度减小,为易错点.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
关于物质的用途下列说法正确的是( )
①利用NaHCO3治疗胃酸过多;
②氢氧化铝可以用做耐火材料;
③氢氟酸可以用来刻蚀玻璃;
④纯净的二氧化硅是制备光导纤维的原料;
⑤利用明矾做干燥剂
⑥漂白粉既可做漂白棉麻纸张的漂白剂,又可做游泳池及环境的消毒剂;
⑦四氧化三铁常用作红色油漆和涂料
⑧晶体硅是良好的半导体材料,可以制成光电池.
①利用NaHCO3治疗胃酸过多;
②氢氧化铝可以用做耐火材料;
③氢氟酸可以用来刻蚀玻璃;
④纯净的二氧化硅是制备光导纤维的原料;
⑤利用明矾做干燥剂
⑥漂白粉既可做漂白棉麻纸张的漂白剂,又可做游泳池及环境的消毒剂;
⑦四氧化三铁常用作红色油漆和涂料
⑧晶体硅是良好的半导体材料,可以制成光电池.
| A、①②③④⑤⑥ |
| B、①③④⑥⑧ |
| C、①②④⑥⑦ |
| D、③④⑤⑥⑦⑧ |
一定温度下,将0.1mol HI置于1L某密闭烧瓶中发生反应:2HI(g)?H2(g)+I2(g),下列结论不能说明上述反应达到平衡状态的是( )
| A、烧瓶内气体的颜色不再加深 |
| B、HI的消耗速率与H2的消耗速率之比为2:1 |
| C、I2的生成速率与I2的消耗速率相等 |
| D、烧瓶内气体的质量不变 |
下列说法正确的是( )
| A、若原子X的质子数为a,则X的质量数一定不为a |
| B、若两种元素形成的离子M2-和N+电子层结构相同,则离子半径M2->N+ |
| C、同周期非金属氧化物对应水化物酸性从左到右依次增强 |
| D、由两种元素组成的化合物,若含有离子键,就没有共价键 |
下列叙述不正确的是( )
| A、石油主要是由各种烷烃、环烷烃、芳香烃组成的混合物,没有固定的熔点 |
B、聚乙烯是由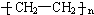 分子组成的化合物,加热至某一温度,则可全部熔化 分子组成的化合物,加热至某一温度,则可全部熔化 |
| C、同质量的乙烯和聚乙烯燃烧后生成的CO2质量相等 |
| D、油脂不是天然高分子化合物 |

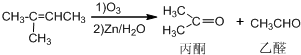
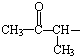 、且属于酯类的同分异构体:
、且属于酯类的同分异构体:
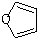 )也可以发生“Diels-Alder反应”,该化学反应方程式为:
)也可以发生“Diels-Alder反应”,该化学反应方程式为: