题目内容
8.某主族元素R的最高正化合价与最低负化合价代数和为4,下列叙述不正确的是( )| A. | R的气态氢化物为H2R | B. | R的最高价氧化物的水化物为H2RO4 | ||
| C. | R一定是第IVA族元素 | D. | R的最高价氧化物为RO3 |
分析 设主族元素R的最高正化合价为x,其最低负价=x-8,则:x+(x-8)=4,解得:x=+6,该元素处于ⅥA族,据此结合元素周期律知识解答.
解答 解:设主族元素R的最高正化合价为x,其最低负价=x-8,则:x+(x-8)=4,解得:x=+6,该元素处于ⅥA族,属于氧族元素,
A.R的最低负化合价为-2,氢化物化学式为H2R,故A正确;
B.R的最高价为+6,则R的最高价氧化物的水化物为H2RO4,如H2SO4,故B正确;
C.根据分析可知,R元素处于ⅥA族,故C错误;
D.R的最高价为+6,则R的最高价氧化物为RO3,故D正确;
故选C.
点评 本题考查原子结构与元素周期律的关系,为高频考点,题目难度不大,侧重于学生的分析能力的考查,关键是清楚元素的最高价和最低负价的关系,注意掌握原子结构与元素周期律的关系.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.化合物X是一种医药中间体,其结构简式如图所示.下列有关化合物X的说法正确的是( )
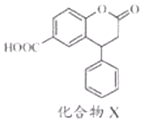

| A. | 分子中两个苯环一定处于同一平面 | |
| B. | 1mol化合物X最多可与8molH2发生加成反应 | |
| C. | 在酸性条件下水解,水解产物只有一种 | |
| D. | 1mol化合物X最多能与2molNaOH反应 |
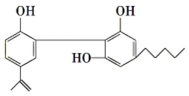
3.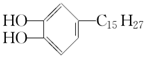 漆酚是我国特产漆的主要成分,结构如图所示:苯环侧链烃基为链状,则下列说法错误的是( )
漆酚是我国特产漆的主要成分,结构如图所示:苯环侧链烃基为链状,则下列说法错误的是( )
 漆酚是我国特产漆的主要成分,结构如图所示:苯环侧链烃基为链状,则下列说法错误的是( )
漆酚是我国特产漆的主要成分,结构如图所示:苯环侧链烃基为链状,则下列说法错误的是( )| A. | 能与FeCl3溶液发生显色反应 | |
| B. | 能使酸性KMnO4溶液褪色 | |
| C. | 能与NaHCO3溶液反应放出CO2 | |
| D. | 1mol漆酚与足量浓溴水反应最多消耗5molBr2 |
17.对Na、Mg、Al的有关性质的叙述正确的是( )
| A. | 碱性:NaOH<Mg(OH)2<Al(OH)3 | B. | 价电子数:Na<Mg<Al | ||
| C. | 电负性:Na>Mg>Al | D. | 第一电离能:Na<Mg<Al |
18.下列A、B、C、D四个同学的陈述完全正确的是( )
| A. | NaCl:我是离子化合物,含有极性键 | |
| B. | H2O:我1mol中含有2mol非极性键 | |
| C. | KOH:既含有离子键,又含有极性共价键 | |
| D. | NaNO3:我是含有离子键的共价化合物 |
 运动员服用兴奋剂的现象在世界大赛中时有发生,某种兴奋剂的结构如图.
运动员服用兴奋剂的现象在世界大赛中时有发生,某种兴奋剂的结构如图.


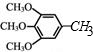 )是重要的医药中间体,利用甲苯为原料合成3,4,5-三甲氧基甲苯的路线如下:
)是重要的医药中间体,利用甲苯为原料合成3,4,5-三甲氧基甲苯的路线如下: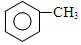 $\stackrel{Br_{2}}{→}$A$\stackrel{NaOH}{→}$
$\stackrel{Br_{2}}{→}$A$\stackrel{NaOH}{→}$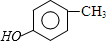 $→_{CH_{3}OH}^{Br_{2}}$B$→_{CH_{3}ONa}^{CuCl,DMF}$
$→_{CH_{3}OH}^{Br_{2}}$B$→_{CH_{3}ONa}^{CuCl,DMF}$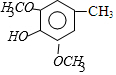 $\stackrel{NaOH}{→}$C$\stackrel{(CH_{3})_{2}SO_{4}}{→}$
$\stackrel{NaOH}{→}$C$\stackrel{(CH_{3})_{2}SO_{4}}{→}$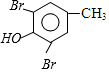 ,C的结构简式为
,C的结构简式为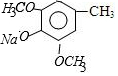 .
.