题目内容
2.某有机物和过量钠反应生成气体VaL,另一份等质量的该有机物和碳酸氢钠反应生成VbL气体(同温同压),若Va=Vb,则该有机物可能是( )| A. | HOCH2CH2COOH | B. | CH3COOH | ||
| C. | HOOC-COOH | D. | 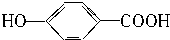 |
分析 有机物和足量的钠反应,该有机物中可能含有-OH或-COOH或-OH、-COOH,该机物与足量的小苏打溶液反应,说明该有机物含有-COOH.有机物与钠反应、与碳酸氢钠反应,二者生成的气体体积相等,则有机物中羧基数目与羟基数目相等,以此解答该题.
解答 解:有机物和足量的钠反应,该有机物中可能含有-OH或-COOH或-OH、-COOH,该机物与足量的小苏打溶液反应,说明该有机物含有-COOH.有机物与钠反应、与碳酸氢钠反应,二者生成的气体体积相等,则有机物中羧基数目与羟基数目相等.
A.HOCH2CH2COOH中羧基与羟基数目相等,该有机物与钠反应、与碳酸氢钠反应,二者生成的气体体积相等,故A正确;
B.CH3COOH中不含羟基,该有机物与钠反应、与碳酸氢钠反应,二者生成的气体体积之比为1:2,故B错误;
C.HOOC-COOH中不含羟基,该有机物与钠反应、与碳酸氢钠反应,二者生成的气体体积之比为1:2,故C错误;
D.含有1个羟基、1个羧基,则该有机物与钠反应、与碳酸氢钠反应,二者生成的气体体积相等,故D正确.
故选AD.
点评 本题考查醇、羧酸的性质与有机物结构推断等,为高频考点,难度不大,清楚醇、羧酸的性质是解题关键,注意基础知识的掌握.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.下列实验现象以及结论正确的是( )
| A | 向盐酸酸化的Ba(NO3)2溶液中通入SO2 | 有白色沉淀生成 | BaSO3难溶于酸 |
| B | 向等浓度的KCl、Kl混合液中滴加AgNO3溶液 | 先出现白色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 溴乙烷与NaOH水溶液共热后,加HNO3酸化,滴加AgNO3溶液 | 出现淡黄色沉淀 | 溴乙烷含溴元素 |
| D | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
| A. | A | B. | B | C. | C | D. | D |
13.某短周期金属元素原子核外最外层电子数是最内层电子数的1.5倍,下列说法正确的是( )
| A. | 该元素的单质性质活泼,具有较强的还原性,可以用于某些金属冶炼 | |
| B. | 该元素的单质常温下不与浓硫酸反应 | |
| C. | 该元素的单质无需特别保存,因为其性质稳定,不易与空气成分反应 | |
| D. | 该元素的最高价氧化物对应的水化物只能与酸反应 |
10. 在固态金属氧化物电解池中,高温电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
 在固态金属氧化物电解池中,高温电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )| A. | Y是电源的正极 | |
| B. | 阴极的反应式是:H2O+2eˉ═H2+O2ˉ,CO2+2e-═CO+O2- | |
| C. | 总反应可表示为:H2+CO2═H2+CO | |
| D. | 阴、阳两极生成的气体的物质的量之比是2:1 |
17.分类是学习和研究化学的一种重要方法,下列分类合理的是( )
| A. | Na2CO3和Na2O2都属于盐 | B. | KOH和KHCO3都属于碱 | ||
| C. | H2SO4和H3PO4都属于酸 | D. | Na2O和Na2SiO3都属于氧化物 |
14.盐A与酸B反应,可放出有气味的气体C,C与NaOH反应生成A;C最终可氧化生成D;D溶于水生成B,则A、B分别是( )
| A. | Na2S和HCl | B. | Na2S和H2SO4 | C. | Na2SO3和HCl | D. | Na2SO3和H2SO4 |
11.某溶液中含有大量的下列离子:Fe3+、SO42-、Al3+和M,经测定Fe3+、SO42-、Al3+和M的物质的量之比为2:4:1:1,则M可能是下列中的( )
| A. | Na+ | B. | OH- | C. | Cl- | D. | S2- |
12.化学与人类生产、生活密切相关,下列说法正确的是( )
| A. | 有机玻璃受热软化,易于加工成型,是一种硅酸盐材料 | |
| B. | 煤的气化是物理变化,是高效、清洁地利用煤的重要途径 | |
| C. | 纯银器在空气中久置变黑是因为发生了电化学腐蚀 | |
| D. | 硫酸亚铁片和维生素C同时服用,能增强治疗缺铁性贫血的效果 |