题目内容
怎样以H2O、H218O、空气、乙烯为原料制取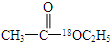 .写出有关反应的化学方程式.
.写出有关反应的化学方程式.
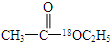 .写出有关反应的化学方程式.
.写出有关反应的化学方程式.考点:乙酸乙酯的制取
专题:有机反应
分析:采用逆推法分析,乙酸乙酯水解得到乙酸和乙醇,乙酸可由乙醛氧化得到,乙醛可由乙醇氧化得到,乙醇可由乙烯和水加成得到,写出方程式即可.
解答:
解:采用逆推法分析,乙酸乙酯水解得到乙酸和乙醇,乙酸可由乙醛氧化得到,乙醛可由乙醇氧化得到,乙醇可由乙烯和水加成得到,故有关的方程式为:CH2=CH2+H2O
CH3CH2OH,CH2=CH2+H218O
CH3CH218OH,
2CH3CH2OH+O2
2CH3CHO+2H2O,2CH3CHO+O2
2CH3COOH,CH3COOH+CH3CH218OH
CH3CO18OCH2CH3+H2O;
答:有关方程式为:CH2=CH2+H2O
CH3CH2OH,CH2=CH2+H218O
CH3CH218OH,
2CH3CH2OH+O2
2CH3CHO+2H2O,2CH3CHO+O2
2CH3COOH,CH3COOH+CH3CH218OH
CH3CO18OCH2CH3+H2O.
| 催化剂 |
| 催化剂 |
2CH3CH2OH+O2
| Cu |
| △ |
| 催化剂 |
| 浓硫酸 |
| △ |
答:有关方程式为:CH2=CH2+H2O
| 催化剂 |
| 催化剂 |
2CH3CH2OH+O2
| Cu |
| △ |
| 催化剂 |
| 浓硫酸 |
| △ |
点评:本题考察了有机合成,较简单,按逆推法分析,按正推法写出方程式,注意反应条件.

练习册系列答案
相关题目
在下列实验中,不能达到目的是( )
| A、Fe与Cl2反应生成FeCl3,Fe与S反应生成FeS,确定非金属性:Cl>S |
| B、用石墨作电极,电解Mg(NO3)2、Cu(NO3)2的混合溶液,确定铜、镁的金属活动性强弱 |
| C、进行H2O和H2S的热分解实验,确定硫和氧两种元素的非金属性强弱 |
| D、测定NaCl和NaF溶液的pH,确定F、Cl两元素非金属性的强弱 |
将铜投入稀硫酸中不能溶解,但向这种稀硫酸中加入下列某种物质后,发现铜能逐渐溶解,溶液逐渐变成蓝色,并可见有气体产生.则向这种稀硫酸中加入的物质是( )
| A、盐酸 | B、硝酸钾 |
| C、氯化钡 | D、氯化铁 |
一定量的混合气体在密闭容器中发生如下反应:mA(g)+nB(g)?pC(g),达平衡后,保持温度不变,将容器的体积缩小为原来的
,当达到新平衡时,测得C的浓度为原来的1.9倍.则下列叙述中正确的是( )
| 1 |
| 2 |
| A、m+n>p |
| B、A的转化率增大 |
| C、平衡逆向移动 |
| D、C的体积百分含量增大 |
下列有关化学反应速率的说法中正确的是( )
| A、氢气与氮气能够缓慢地反应生成氨气,使用合适的催化剂可以提高化学反应速率 |
| B、等质量的锌粉和锌片与相同体积、相同浓度的盐酸反应,反应速率相等 |
| C、用铁片与硫酸制备氢气时,浓硫酸可以加快产生氢气的速率 |
| D、增大反应CO2(g)+H2(g)═CO(g)+H2O(g)的压强,反应速率不变 |
 某化学兴趣小组在进行钠在空气中燃烧的实验,请写出钠在氧气中燃烧的化学方程式:
某化学兴趣小组在进行钠在空气中燃烧的实验,请写出钠在氧气中燃烧的化学方程式:
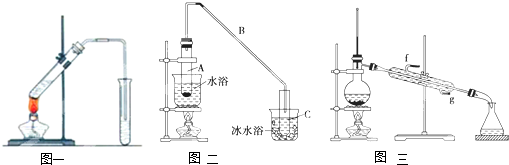
 为了确认CH3COOH、H2CO3和H2SiO3的酸性强弱,有人设计用如图所示装置,一次实验达到目的(不能再选用其他酸性溶液).
为了确认CH3COOH、H2CO3和H2SiO3的酸性强弱,有人设计用如图所示装置,一次实验达到目的(不能再选用其他酸性溶液).