题目内容
已知A、B、C、D、E是短周期中原子序数依次增大的5种元素,其中A与B形成可使红色石蕊试纸变蓝的气体,C的最高价氧化物对应水化物呈强碱性,D的离子半径是所在同周期元素简单离子半径中最小的,B与E可形成三角锥型分子且每个原子最外层都满足8电子稳定结构.
1B在元素周期表中的位置为第 周期 族,BA3空间构型为 ;
(2)物质甲是C在氧气中燃烧的产物,甲的电子式为 ; C、D、E各自形成的简单离子半径由小到大的顺序为 (用离子符号表示)
(3)E的同族元素的氢化物中沸点最低的是 (写分子式)
(4)物质乙由A和B元素组成,分子中含18个电子.常温常压下,3.2g液态乙在空气中燃烧生成B的单质,同时放出aKJ热量,该反应的热化学方程式为 .
(5)将10.8g D单质与15.6g甲混合后,完全溶于水中得1L溶液,所得溶液中溶质的物质的量浓度为 (溶液体积变化忽略不计),产生的气体在标况下体积为 L.
1B在元素周期表中的位置为第
(2)物质甲是C在氧气中燃烧的产物,甲的电子式为
(3)E的同族元素的氢化物中沸点最低的是
(4)物质乙由A和B元素组成,分子中含18个电子.常温常压下,3.2g液态乙在空气中燃烧生成B的单质,同时放出aKJ热量,该反应的热化学方程式为
(5)将10.8g D单质与15.6g甲混合后,完全溶于水中得1L溶液,所得溶液中溶质的物质的量浓度为
考点:位置结构性质的相互关系应用
专题:
分析:A与B形成可使红色石蕊试纸变蓝的气体,该气体为氨气,根据原子序数大小可知A为H元素、B为N元素;C的最高价氧化物对应水化物呈强碱性,则C为金属元素,C的原子序数大于N元素,则C位于第三周期,所以C、D、E都位于第三周期;第三周期中离子半径最小的一定为金属元素、且是金属元素中核电荷数最大的,则D为Al元素;B与E可形成三角锥型分子且每个原子最外层都满足8电子稳定结构,B为N元素,E元素为第三周期-1价元素,则E为Cl元素,据此进行解答.
解答:
解:A与B形成可使红色石蕊试纸变蓝的气体,该气体为氨气,根据原子序数大小可知A为H元素、B为N元素;C的最高价氧化物对应水化物呈强碱性,则C为金属元素,C的原子序数大于N元素,则C位于第三周期,所以C、D、E都位于第三周期;第三周期中离子半径最小的一定为金属元素、且是金属元素中核电荷数最大的,则D为Al元素;B与E可形成三角锥型分子且每个原子最外层都满足8电子稳定结构,则E为Cl元素,
(1)根据分析可知,B为N元素,在元素周期表中的位置为第二周期ⅤA族;BA3是氨气,空间构型为三角锥形,
故答案为:二;ⅤA;三角锥形;
(2)C为Na,C在氧气中燃烧生成过氧化钠,过氧化钠的电子式为: ;
;
C、D、E形成的简单离子分别是Na+、Al3+、Cl-,三种微粒中Cl-核外有三个电子层,离子半径最大,Na+、Al3+核外电子层结构相同,核内质子数不同,质子数越多,离子半径越小,故Al3+<Na+,故三种微粒半径由小到大的顺序为:Al3+<Na+<Cl-,
故答案为: ;Al3+<Na+<Cl-;
;Al3+<Na+<Cl-;
(3)E的同族元素的氢化物有HF、HCl、HBr、HI,组成和结构相同,但是由于HF分子间形成了氢键,故沸点高于其余三种,在其余三种氢化物中,沸点的高低与相对分子量有关,相对分子量越大,沸点越高,故沸点最低的是HCl,
故答案为:HCl;
(4)物质乙由A和B元素组成,分子中含18个电子,物质乙为N2H4,3.2g 的N2H4的物质的量为0.1mol,则1molN2H4燃烧放出的热量为10aKJ,所以热化学方程式为:N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=-10akJ?mol-1,
故答案为:N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=-10akJ?mol-1;
(5)D单质为金属铝,甲为工业化和,发生的反应为:2Na2O2+2H2O═4NaOH+O2↑、2Al+2H2O+2NaOH═2NaAlO2+3H2↑,
A15.6gNa2O2的物质的量为:
=0.2mol,10.8gAl的物质的量为:
=0.4mol,根据反应可知金属铝恰好与氢氧化钠完全反应生成0.4mol的NaAlO2,故溶液的浓度为:
=0.4mol/L;
根据反应可知,0.2mol过氧化钠与水反应生成氧气的物质的量为0.1mol,0.4mol铝与氢氧化钠溶液反应生成0.6mol氢气,则产生的气体总的物质的量为0.6mol+0.1mol=0.7mol,标况下0.7mol气体体积为:22.4L/mol×0.7mol=15.68L,
故答案为:0.4mol/L;15.68.
(1)根据分析可知,B为N元素,在元素周期表中的位置为第二周期ⅤA族;BA3是氨气,空间构型为三角锥形,
故答案为:二;ⅤA;三角锥形;
(2)C为Na,C在氧气中燃烧生成过氧化钠,过氧化钠的电子式为:
 ;
;C、D、E形成的简单离子分别是Na+、Al3+、Cl-,三种微粒中Cl-核外有三个电子层,离子半径最大,Na+、Al3+核外电子层结构相同,核内质子数不同,质子数越多,离子半径越小,故Al3+<Na+,故三种微粒半径由小到大的顺序为:Al3+<Na+<Cl-,
故答案为:
 ;Al3+<Na+<Cl-;
;Al3+<Na+<Cl-;(3)E的同族元素的氢化物有HF、HCl、HBr、HI,组成和结构相同,但是由于HF分子间形成了氢键,故沸点高于其余三种,在其余三种氢化物中,沸点的高低与相对分子量有关,相对分子量越大,沸点越高,故沸点最低的是HCl,
故答案为:HCl;
(4)物质乙由A和B元素组成,分子中含18个电子,物质乙为N2H4,3.2g 的N2H4的物质的量为0.1mol,则1molN2H4燃烧放出的热量为10aKJ,所以热化学方程式为:N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=-10akJ?mol-1,
故答案为:N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=-10akJ?mol-1;
(5)D单质为金属铝,甲为工业化和,发生的反应为:2Na2O2+2H2O═4NaOH+O2↑、2Al+2H2O+2NaOH═2NaAlO2+3H2↑,
A15.6gNa2O2的物质的量为:
| 15.6g |
| 78g/mol |
| 10.8g |
| 27g/mol |
| 0.4mol |
| 1L |
根据反应可知,0.2mol过氧化钠与水反应生成氧气的物质的量为0.1mol,0.4mol铝与氢氧化钠溶液反应生成0.6mol氢气,则产生的气体总的物质的量为0.6mol+0.1mol=0.7mol,标况下0.7mol气体体积为:22.4L/mol×0.7mol=15.68L,
故答案为:0.4mol/L;15.68.
点评:本题考查了位置、结构与性质关系的综合应用,题目难度中等,正确推断各元素名称为解答关键,注意熟练掌握元素周期表结构、元素周期律内容,试题侧重考查学生的分析、理解能力及灵活应用基础知识的能力.

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
甲、乙两烧杯中各盛有100mL 3mol/L的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后收集到相同条件下气体体积比为甲:乙=1:2,则加入铝粉的质量为( )
| A、5.4g | B、3.6g |
| C、2.7g | D、1.6g |
化合物A、B、C都只含有两种元素,且A、B均含X元素,已知一定条件下可发生反应:A+B→C+X,X是一种单质,由此可知( )
| A、X一定是金属元素 |
| B、X一定是非金属元素 |
| C、X可能是金属元素,也可能是非金属元素 |
| D、A、B中X的化合价均高于0 |
在2L密闭容器中把4molA和2mol B混合,在一定条件下发生反应3A(g)+2B(g)?zC(g)+2D(g).2min后反应达到平衡时生成1.6mol C,又测得反应速率v(D)=0.2mol/(L?min).则下列说法正确的是( )
| A、z=4 | ||
| B、B物质的转化率是20% | ||
| C、A的平衡浓度是1.6 mol/L | ||
D、平衡时气体压强是原来的
|
下列物质中,所含主要成分不同于其他三种的是( )
| A、沼气 | B、煤气 |
| C、天然气 | D、煤矿内瓦斯 |
关于下列实验的叙述合理的是( )
| A、某氢化物的溶液能使石蕊试液变蓝,该氢化物一定是氨气 |
| B、将某气体通入品红溶液中,品红溶液褪色,该气体一定是SO2 |
| C、配制硫酸亚铁溶液时应将硫酸亚铁固体溶于浓硫酸中,再稀释至所需浓度,以防止水解 |
| D、配制银氨溶液应将稀氨水逐滴滴入到硝酸银溶液中至产生的沉淀刚好溶解 |
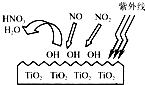 还原剂还原法、光催化氧化法、电化学吸收法是减少氮氧化物排放的有效措施.
还原剂还原法、光催化氧化法、电化学吸收法是减少氮氧化物排放的有效措施.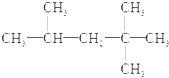 某有机物化合物A的结构简式如图完成下列问题:
某有机物化合物A的结构简式如图完成下列问题: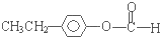 、
、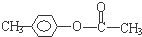 ,写出另外两种的结构简式:
,写出另外两种的结构简式: