题目内容
实验是研究化学的基础,下列关于实验操作的叙述中正确的是( )
| A、向盛有沸水的烧杯中滴加FeCl3溶液并长时间煮沸,制备Fe(OH)3胶体 |
| B、某溶液用盐酸酸化无明显现象,再滴加氯化钡溶液有白色沉淀生成,说明溶液中有SO42- |
| C、钠保存在盛有煤油的细口试剂瓶中 |
| D、配制0.1mol/L的H2SO4溶液时,将量取的浓硫酸倒入容量瓶中加水稀释至刻度线 |
考点:硫酸根离子的检验,化学试剂的存放,配制一定物质的量浓度的溶液
专题:实验评价题
分析:A.向盛有沸水的烧杯中滴加FeCl3溶液并长时间煮沸,生成的胶体在加热条件下发生聚沉,形成红褐色沉淀;
B.加入盐酸后排除了干扰离子,再加入氯化钡,若生成了白色沉淀,该白色沉淀为硫酸钡,则原溶液中一定含有硫酸根离子;
C.钠与空气中水、氧气反应,钠保存在盛有煤油的广口试剂瓶中;
D.浓硫酸在稀释过程中放出热量,需要冷却至室温后再转移到容量瓶中;
B.加入盐酸后排除了干扰离子,再加入氯化钡,若生成了白色沉淀,该白色沉淀为硫酸钡,则原溶液中一定含有硫酸根离子;
C.钠与空气中水、氧气反应,钠保存在盛有煤油的广口试剂瓶中;
D.浓硫酸在稀释过程中放出热量,需要冷却至室温后再转移到容量瓶中;
解答:
解:A.制备氢氧化铁胶体时,当溶液呈红褐色时应停止加热,否则生成的胶体在加热条件下发生聚沉,形成红褐色沉淀,故A错误;
B.向某溶液中加入足量的盐酸无明显现象,说明溶液中不存在银离子、碳酸根离子,然后再加入BaCl2溶液,产生白色沉淀,该白色沉淀为硫酸钡,证明原溶液中存在硫酸根离子,故B正确;
C.金属钠化学性质活泼,能够与氧气、水发生反应,且密度比煤油的密度小,所以金属钠保存在煤油中,因钠是块状固体,应保存在盛有煤油的广口试剂瓶中,故C错误;
D.容量瓶上只标有容量瓶的规格和容量瓶瓶颈有一刻度线,受热会出现热胀冷缩现象,所以不能将量取的浓硫酸倒入容量瓶中加水稀释至刻度线,故D错误;
故选B.
B.向某溶液中加入足量的盐酸无明显现象,说明溶液中不存在银离子、碳酸根离子,然后再加入BaCl2溶液,产生白色沉淀,该白色沉淀为硫酸钡,证明原溶液中存在硫酸根离子,故B正确;
C.金属钠化学性质活泼,能够与氧气、水发生反应,且密度比煤油的密度小,所以金属钠保存在煤油中,因钠是块状固体,应保存在盛有煤油的广口试剂瓶中,故C错误;
D.容量瓶上只标有容量瓶的规格和容量瓶瓶颈有一刻度线,受热会出现热胀冷缩现象,所以不能将量取的浓硫酸倒入容量瓶中加水稀释至刻度线,故D错误;
故选B.
点评:本题考查了胶体的制备、常见离子的检验、钠的保存、容量瓶的使用,题目难度不大,注意掌握常见离子的性质及检验方法,在检验离子存在时,需要排除干扰保证检验方案的严密性.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
在一定条件下,跟酸、碱、盐都能反应的物质是( )
| A、K2O |
| B、Na2CO3 |
| C、CaCO3 |
| D、CO2 |
 对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法正确的是( )
对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法正确的是( )①Zn是负极
②电子由Zn经外电路流向Cu
③Zn极发生氧化反应生成Zn2+
④H+在溶液中由Cu极向Zn极迁移.
| A、①②④ | B、②③④ |
| C、①②③ | D、①②③④ |
关于蛋白质的叙述错误的是( )
| A、浓HNO3溅在皮肤上,使皮肤呈黄色,是由于浓HNO3和蛋白质发生颜色反应 |
| B、蛋白质溶液中加入饱和(NH4)2SO4溶液,蛋白质析出,再加水也不溶解 |
| C、蛋白质水解的最终产物是氨基酸 |
| D、高温灭菌的原理是加热后使蛋白质变性,从而使细菌死亡 |
有关下列四个装置的描述正确的是( )
A、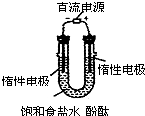 工作时溶液中OH-向阳极移动,因此阳极附近溶液先变红色 |
B、 装置中Zn作正极,Cu作负极 |
C、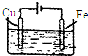 可实现对铁制品表面镀铜 |
D、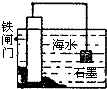 可实现对铁闸门保护 |
下列除去杂质的方法正确的是( )
| A、除去CO2中混有的CO:用澄清石灰水洗气 |
| B、除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤 |
| C、除去BaCO3固体中混有的BaSO4:加过量盐酸后,过滤、洗涤 |
| D、除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤 |
分类是学习化学的重要方法.下列归纳正确的是( )
| A、SO2、SiO2、CO均为酸性氧化物 |
| B、纯碱、烧碱、熟石灰都属于碱类 |
| C、氨气、冰醋酸、食盐均为电解质 |
| D、冰和干冰既是纯净物又是化合物 |
 如图所示的试管内,液体分层,已知一层是水,另一层是某未知有机物,下列操作不能确定哪一层是水层的为( )
如图所示的试管内,液体分层,已知一层是水,另一层是某未知有机物,下列操作不能确定哪一层是水层的为( )