题目内容
9.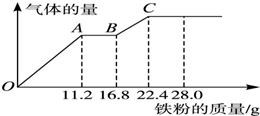 某稀硫酸和稀硝酸的混合溶液200mL,向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.
某稀硫酸和稀硝酸的混合溶液200mL,向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.则BC段气体是产生的气体是H2;OA段离子反应方程式为Fe+4H++NO3-═Fe3++NO↑+2H2O,c(H2SO4)为2mol/L.
分析 由图象可知,由于铁过量,OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段发生反应为:Fe+2Fe3+=3Fe2+,BC段发生反应为:Fe+2H+=Fe2++H2↑;最终消耗22.4gFe,溶液中溶质为FeSO4,根据Fe元素守恒可以计算n(FeSO4),再根据硫酸根守恒计算每一份溶液中n(H2SO4),进而计算硫酸的物质的量浓度.
解答 解:由图象可知,由于铁过量,OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段发生反应为:Fe+2Fe3+=3Fe2+,BC段发生反应为:Fe+2H+=Fe2++H2↑.
最终消耗22.4gFe,其物质的量为$\frac{22.4g}{56g/mol}$=0.4mol,溶液中溶质为FeSO4,根据Fe元素守恒可n(FeSO4)=n(Fe)=0.4mol,再根据硫酸根守恒,每一份溶液中n(H2SO4)=n(FeSO4)=0.4mol,故意硫酸的物质的量浓度为$\frac{0.4mol}{0.2L}$=2mol/L;
故答案为:H2;Fe+4H++NO3-═Fe3++NO↑+2H2O;2mol/L.
点评 本题以图象为载体,考查有关金属和酸反应的计算题,难度中等,关键根据图象分析各段发生的反应,注意与铁的反应中硝酸全部起氧化剂作用,侧重于考查学生的分析能力和计算能力.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
19.下列有关甲烷的说法中,不正确的是( )
| A. | 不能使酸性高锰酸钾溶液褪色 | B. | 可以用排水法或向下排空气法收集 | ||
| C. | 是最简单的有机物 | D. | 能使溴水褪色 |
20.有8种物质:①乙烷、②乙烯、③乙炔、④苯、⑤甲苯、⑥溴乙烷、⑦聚乙烯、⑧丁二烯,其中既不能使KMnO4溶液褪色,也不能与溴水发生化学反应的是( )
| A. | ①②③⑤ | B. | ④⑥⑦⑧ | C. | ①④⑥⑦ | D. | ②③⑤⑧ |
17.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 23 g钠在氧气中完全燃烧失电子数为0.5NA | |
| B. | 46gNO2和N2O4混合气体中含有氮原子数为1NA~2NA | |
| C. | 1 mol Cl2参加反应转移电子数可能为2NA | |
| D. | 含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol/L |
4.某学习小组通过下列装置探究MnO2与FeCl3•6H2O能否反应产生Cl2.
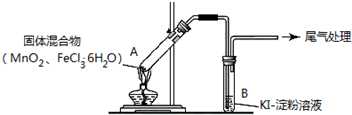
实验操作和现象:
(1)现象 i 中的白雾是盐酸小液滴,形成白雾的原因是FeCl3•6H2O 受热水解,生成HCl 气体,同时受热失去结晶水,HCl和H2O 结合形成盐酸小液滴.
(2)分析现象 ii,该小组探究黄色气体的成分,实验如下:
a.加热FeCl3•6H2O,产生白雾和黄色气体.
b.用KSCN 溶液检验现象 ii 和a 中的黄色气体,溶液均变红.通过该实验说明现象 ii 中黄色气体含有FeCl3.
(3)除了氯气可使B 中溶液变蓝外,推测还可能的原因是:
①实验b 检出的气体使之变蓝,反应的离子方程式是2Fe3++2I-=2Fe2++I2.实验证实推测成立.
②溶液变蓝的另外一种原因是:在酸性条件下,装置中的空气使之变蓝.通过进一步实验确认了这种可能性,其实验方案是另取一支试管,向其中加入KI淀粉溶液,再滴入几滴 HCl溶液,在空气中放置,若一段时间后溶液变蓝则推测成立.
(4)为进一步确认黄色气体是否含有 Cl2,小组提出两种方案,均证实了Cl2的存在.
①方案1 的洗气瓶C中盛放的试剂是饱和NaCl溶液.
②方案2 中检验 Fe 2+的原因是排除Fe3+将Br-氧化成Br2 的可能性.
(5)将A 中产物分离得到Fe2O3和MnCl2,A 中发生反应的化学方程式是3MnO2+4FeCl3•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+3MnCl2+3Cl2↑+24H2O.

实验操作和现象:
| 操作 | 现象 |
| 点燃酒精灯,加热 | i.A中部分固体溶解,上方出现白雾 ii.稍后,产生黄色气体,管壁附着黄色液滴 iii.B中溶液变蓝 |
(2)分析现象 ii,该小组探究黄色气体的成分,实验如下:
a.加热FeCl3•6H2O,产生白雾和黄色气体.
b.用KSCN 溶液检验现象 ii 和a 中的黄色气体,溶液均变红.通过该实验说明现象 ii 中黄色气体含有FeCl3.
(3)除了氯气可使B 中溶液变蓝外,推测还可能的原因是:
①实验b 检出的气体使之变蓝,反应的离子方程式是2Fe3++2I-=2Fe2++I2.实验证实推测成立.
②溶液变蓝的另外一种原因是:在酸性条件下,装置中的空气使之变蓝.通过进一步实验确认了这种可能性,其实验方案是另取一支试管,向其中加入KI淀粉溶液,再滴入几滴 HCl溶液,在空气中放置,若一段时间后溶液变蓝则推测成立.
(4)为进一步确认黄色气体是否含有 Cl2,小组提出两种方案,均证实了Cl2的存在.
| 方案1 | 在A、B 间增加盛有某种试剂的洗气瓶C | B中溶液变为蓝色 |
| 方案2 | 将B 中KI淀粉溶液替换为NaBr 溶液;检验 Fe 2+ | B中溶液呈浅橙红色;未检出Fe 2+ |
②方案2 中检验 Fe 2+的原因是排除Fe3+将Br-氧化成Br2 的可能性.
(5)将A 中产物分离得到Fe2O3和MnCl2,A 中发生反应的化学方程式是3MnO2+4FeCl3•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+3MnCl2+3Cl2↑+24H2O.
14.为了提纯下列物质(括号内为杂质),有关除杂试剂和分离方法的选择均正确的是( )
| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 溴苯(溴) | 水 | 分液 |
| B | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| C | 苯(苯酚) | NaOH溶液 | 分液 |
| D | 甲烷(乙烯) | KMnO4酸性溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
1.下列鉴别方法不可行的是( )
| A. | 用水鉴别乙醇、甲苯和溴苯 | |
| B. | 用溴水鉴别乙烯和SO2 | |
| C. | 用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 | |
| D. | 用酸性高锰酸钾溶液鉴别苯、乙烯和己烷 |
18.鉴别二氧化硫和乙烯两种气体,下列方法或所选试剂中不可行的是( )
| A. | 可燃性实验 | B. | 酸性高锰酸钾 | C. | 澄清石灰水 | D. | 品红试液 |