题目内容
用18 mol·L-1 浓硫酸配制100 mL 3.0 mol·L-1 稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③溶解 ④ ⑤转移、洗涤
⑥定容、摇匀 ⑦装瓶贴标签。
完成下列问题:
(1)所需浓硫酸的体积是 ,量取浓硫酸所用的量筒的规格是 (从下列中选用A.10 mL B.25 mL C.50 mL D.100 mL
(2)第③步实验的操作是 。
(3)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“ 偏小”“ 无影响”填写)
A.所用的浓硫酸长时间放置在密封不好的容器中_______________________;
B.容量瓶用蒸馏水洗涤后残留有少量的水________________;
C.所用过的烧杯、玻璃棒未洗涤________________;
D.定容时俯视刻度线________________。
(1)16.7 mL ,B;
(2)先向烧杯加入30mL (或适量)蒸馏水,然后将浓硫酸沿烧杯内壁缓慢倒入烧杯中,并用玻璃棒搅拌。
(3)A.偏小 ;B.无影响 ;C.偏小 ;D.偏大。
【解析】
试题分析:物质的溶液在稀释过程中溶质的物质的量不变,所以c1·V1=c2·V2。所以V1=(100 mL ×3.0 mol/L)÷18 mol/L=16.7 mL;量取浓硫酸所用的量筒的规格应该与量取的液体的体积越接近,误差越小,所以应该选择25 mL的量筒,选项是B;(2)第③步实验的操作物质的溶解,即硫酸的稀释,具体操作是先向烧杯加入30mL (或适量)蒸馏水,然后将浓硫酸沿烧杯内壁缓慢倒入烧杯中,并用玻璃棒搅拌。(3)A.浓硫酸有吸水性,放置时间长了溶液变稀,所以所用的浓硫酸长时间放置在密封不好的容器中,由于变稀溶质偏少,所配制的溶液的浓度就偏小;B.容量瓶用蒸馏水洗涤后残留有少量的水,由于溶质的物质的量不变,最后定容时溶液的体积也不变,所以对溶液的浓度不会有影响;C.所用过的烧杯、玻璃棒未洗涤,则溶质的物质的量减少,因此所配制的溶液的浓度就偏小;D.定容时俯视刻度线,则溶液的体积就偏小,那么溶液的浓度就偏大。
考点:考查物质的量浓度的溶液的配制的知识,主要包括仪器的选择、操作方法、误差分析。

 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案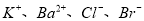
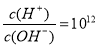 的溶液中:
的溶液中: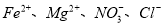
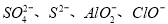
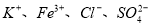
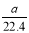 mo1·L-1 B.
mo1·L-1 B.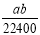 mol·L-1
mol·L-1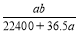 mol·L-1 D.
mol·L-1 D.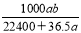 mol·L-1
mol·L-1 2SO3(g) △H=-197kJ/mol。在25℃时,向恒压密闭容器中通入2 mol SO2和1 mol O2,达到平衡时放出热量a1;若25℃时在此恒压密闭容器中只通入1 mol SO2和0.5 mol O2,达到平衡时放出热量a2。则下列关系正确的是( )
2SO3(g) △H=-197kJ/mol。在25℃时,向恒压密闭容器中通入2 mol SO2和1 mol O2,达到平衡时放出热量a1;若25℃时在此恒压密闭容器中只通入1 mol SO2和0.5 mol O2,达到平衡时放出热量a2。则下列关系正确的是( )