题目内容
5.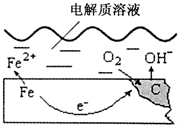 如图是钢铁在潮湿空气里发生电化学腐蚀的示意图,发生的反应为:2Fe+2H2O+O2═2Fe(OH)2.Fe(OH)2继续被氧化为Fe(OH)3,Fe(OH)3脱水生成铁锈.请根据图示,回答下列问题:
如图是钢铁在潮湿空气里发生电化学腐蚀的示意图,发生的反应为:2Fe+2H2O+O2═2Fe(OH)2.Fe(OH)2继续被氧化为Fe(OH)3,Fe(OH)3脱水生成铁锈.请根据图示,回答下列问题:| 物质 | 熔点/°C | 沸点/°C | 密度/g•cm-3 | 溶解性 |
| A | -11.5 | 198 | 1.11 | A、B互溶,且均易溶于水 |
| B | 17.9 | 290 | 1.26 |
(2)写出负极的电极反应式Fe-2e-=Fe2+.
(3)工业上,常在钢铁设备的表面涂一层油,其作用是A.
A.减少钢铁与空气和水的接触,防止在钢铁表面形成微小原电池
B.隔绝钢铁与空气和水的接触,阻止在钢铁表面形成微小电解池
C.润滑设备,防止灰尘污染
D.防止人为接触设备,避免设备腐蚀
(4)如果将长期浸泡在河水中的钢铁闸门与外电源连接防腐,应将闸门连接外部直流电源的负极.
分析 (1)钢铁在潮湿空气里发生电化学腐蚀时,铁做负极,碳作正极;
(2)在中性环境中,铁失去电子生成二价铁离子;
(3)钢铁设备的表面涂一层油是为了隔绝空气和水;
(4)钢铁闸门需要保护,作阴极,与负极相连.
解答 解:(1)上述电化学腐蚀中,铁发生氧化反应,做负极,碳做正极,故答案为:正;
(2)在中性环境中,铁失去电子生成二价铁离子,电极反应式为:Fe-2e-=Fe2+,故答案为:Fe-2e-=Fe2+;
(3)钢铁设备的表面涂一层油是为了隔绝空气和水,从而不能发生电化学腐蚀,即阻止在钢铁表面形成微小原电池,故选A;
(4)钢铁闸门需要保护,作阴极,与负极相连,故答案为:负.
点评 本题考查了原电池和电解池的基本原理,书写电极反应式,确定正负极、阴阳极,保护物质不被腐蚀,属于基础题,但为易错点.

练习册系列答案
相关题目
16.下列依据热化学方程式得出的结论正确的是( )
| A. | 已知2H2(g)+O2(g)=2H2O(g);△H=-483.6 kJ•mol-1,则氢气的燃烧热为241.8kJ•mol-1 | |
| B. | 已知C(石墨,s)=C(金刚石,s);△H>0,则金刚石比石墨稳定 | |
| C. | 已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.4kJ•mol-1,则含20.0g溶质的NaOH稀溶液与稀醋酸完全中和,放出的热量小于28.7kJ | |
| D. | 已知:2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2 |
13.对热化学方程式C(s)+H2O(g)═CO(g)+H2(g)△H=+131.3kJ•mol-1最准确的理解是( )
| A. | 1 mol碳和1 mol水蒸气反应生成1 mol CO和1 mol H2,同时吸收131.3 kJ热量 | |
| B. | 1 mol碳和1 mol水反应生成1 molCO和 1 mol H2,同时放出131.3 kJ热量 | |
| C. | 固体碳和水蒸汽反应吸收131.3 kJ热量 | |
| D. | 1个碳原子和1个水分子反应,吸热131.1 kJ |
20.下列说法正确的是( )
| A. | 钢铁发生电化学腐蚀时,负极反应都是Fe-3e-=Fe3+ | |
| B. | 镀锡的铁制品,若发生镀层破损,铁制品比受损前更容易锈蚀 | |
| C. | 铜的金属活动性比铁弱,可在海轮外壳上装上铜块以减缓船体腐蚀 | |
| D. | 钢铁发生吸氧腐蚀时,正极反应是:2H2O+O2+4e-=4OH- |
10.下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是( )
| A. | SO2和Si | B. | CO2和H2O | C. | NaCl和HCl | D. | CCl4和KCl |
17.分类是学习和研究化学的一种重要方法,下列对于Na2O的分类合理的是( )
| A. | 属于盐 | B. | 属于碱 | C. | 属于酸 | D. | 属于氧化物 |
15.下列可以使有色布条褪色的物质是( )
| A. | 久置的氯水 | B. | 次氯酸钠溶液 | C. | 漂白粉溶液 | D. | 氯化钙溶液 |
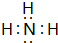 B位于周期表中第二周期ⅦA族.
B位于周期表中第二周期ⅦA族.