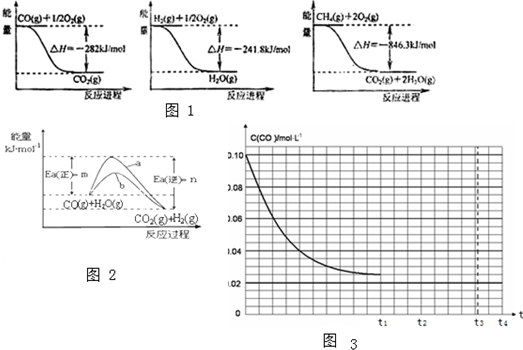
题目内容
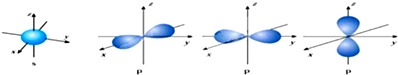
Ⅰ.下面是s能级p能级的原子轨道图,试回答问题:s电子的原子轨道呈 形,每个s能级有 个原子轨道;p电子的原子轨道呈 形,每个p能级有 个原子轨道.
Ⅱ.写出下列元素基态原子的电子排布式:
(1)Ca (2)Kr
(3)Co (4)Ge .
Ⅱ.写出下列元素基态原子的电子排布式:
(1)Ca
(3)Co

考点:原子核外电子的运动状态,原子核外电子排布
专题:原子组成与结构专题
分析:Ⅰ.根据图片中轨道的形状进行分析解答,注意p能级有3个轨道;
Ⅱ.处于最低能量的原子叫做基态原子,基态电子排布遵循能量最低原理、保里不相容原理和洪特规则,根据元素符号,判断元素原子的核外电子数,再根据核外电子排布规律来写,以此解答该题;
Ⅱ.处于最低能量的原子叫做基态原子,基态电子排布遵循能量最低原理、保里不相容原理和洪特规则,根据元素符号,判断元素原子的核外电子数,再根据核外电子排布规律来写,以此解答该题;
解答:
解:Ⅰ.根据图片,s电子的原子轨道呈球形;p电子的原子轨道呈纺锤形,每个p能级有3个原子轨道,且这三个轨道相互垂直,
故答案为:球;纺锤;3;
Ⅱ.Ca元素为20号元素,原子核外有20个电子,所以核外电子排布式为:1s22s22p63s23p64s2,
故答案为:1s22s22p63s23p64s2;
Kr元素为36号元素,原子核外有36个电子,所以核外电子排布式为:1s22s22p63s23p63d104s24p6,
故答案为:1s22s22p63s23p63d104s24p6;
Co元素为27号元素,原子核外有27个电子,所以核外电子排布式为:1s22s22p63s23p63d74s2,
故答案为:1s22s22p63s23p63d74s2;
Ge元素为32号元素,原子核外有32个电子,所以核外电子排布式为:1s22s22p63s23p63d104s24p2,
故答案为:1s22s22p63s23p63d104s24p2;
故答案为:球;纺锤;3;
Ⅱ.Ca元素为20号元素,原子核外有20个电子,所以核外电子排布式为:1s22s22p63s23p64s2,
故答案为:1s22s22p63s23p64s2;
Kr元素为36号元素,原子核外有36个电子,所以核外电子排布式为:1s22s22p63s23p63d104s24p6,
故答案为:1s22s22p63s23p63d104s24p6;
Co元素为27号元素,原子核外有27个电子,所以核外电子排布式为:1s22s22p63s23p63d74s2,
故答案为:1s22s22p63s23p63d74s2;
Ge元素为32号元素,原子核外有32个电子,所以核外电子排布式为:1s22s22p63s23p63d104s24p2,
故答案为:1s22s22p63s23p63d104s24p2;
点评:本题考查了原子轨道形状的判断、基态原子的核外电子排布式等知识点,考查了学生的空间想象能力,元素基态原子的电子排布式须根据核外电子排布规律书写,注意电子处于全满、半满、全空时最稳定,题目难度中等.

练习册系列答案
相关题目
 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A、最简单气态氢化物的热稳定性:R>Q |
| B、最高价氧化物对应水化物的酸性:Q>W |
| C、原子半径:T>Q>R |
| D、Q最高价氧化物形成的晶体熔点很低 |
下列变化属于加成反应的是( )
| A、乙烯通过酸性KMnO4溶液 |
| B、乙醇和浓硫酸共热 |
| C、乙炔使溴水褪色 |
| D、苯酚与浓溴水混合 |