题目内容
11.分子中含有34个氢原子的烷烃分子式为C16H34;在同温同压下与CO2密度相同的烷烃分子式为C3H8;通常情况下为液态的分子中含碳原子数最少的烷烃的分子式是C5H12.分析 烷烃的通式为CnH2n+2,相对分子质量为14n+2,C原子数大于4时为液体,大于17时为固体,以此解答该题.
解答 解:烷烃的通式为CnH2n+2,分子中含有34个氢原子,则2n+2=34,n=16,为C16H34,
在同温同压下与CO2密度相同的烷烃,其相对分子质量为44,则14n+2=44,n=3,为C3H8,
C原子数大于4时为液体,大于17时为固体,则通常情况下为液态的分子中含碳原子数最少的烷烃C原子数为5,为C5H12,
故答案为:C16H34; C3H8; C5H12.
点评 本题考查有机物分子式的确定,为高频考点,侧重股学生的分析能力和计算能力的考查,充分利用烷烃的组成通式进行解答,有利于基础知识的巩固.

练习册系列答案
相关题目
16.下列各种情况下,溶液中可能大量存在的离子组是( )
| A. | 在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×1013的溶液中:NH4+、Ca2+、C1-、K+ | |
| B. | 澄清透明的无色溶液中:K+、Mg2+、NO3-、MnO4- | |
| C. | 使pH试纸呈红色的溶液中:I-、Cl-、NO3-、Na+ | |
| D. | 含有较多的Al3+的溶液中:K+、Ca2+、S2-、Cl- |
19.下列说法不正确的是( )
| A. | 氧化性(酸性溶液):PbO2>Fe3+>S | |
| B. | 还原性(碱性溶液):Fe(OH)2>KCl>Cl2 | |
| C. | 酸性(水溶液):H2S>H2SO4>H2SeO4>HN3 | |
| D. | 热稳定性:CaCO3>FeCO3>Ag2CO3 |
6.下列有关方程式正确的是( )
| A. | 向硫酸亚铁溶液中加入双氧水的离子方程式:Fe2++2H2O+4H+=Fe3++4H2O | |
| B. | 粗硅制备的化学方程式:C+SiO2$\frac{\underline{\;高温\;}}{\;}$CO2↑+Si | |
| C. | 石墨作电极电解CuSO4溶液的离子方程式:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+ | |
| D. | 铁发生吸氧腐蚀时负极上的电极反应式:Fe-3e-=Fe3+ |
20.下列叙述不正确的是( )
| A. | 金属腐蚀的本质是金属原子失去电子而被氧化 | |
| B. | 钢铁吸氧腐蚀的正极反应是:O2+4e-+2H2O═4OH- | |
| C. | 将地下钢管与直流电源的正极相连,用来保护钢管 | |
| D. | 氢氧燃料电池中,氢气在负极发生氧化反应 |
1.观察下列几个装置示意图,有关叙述正确的是( )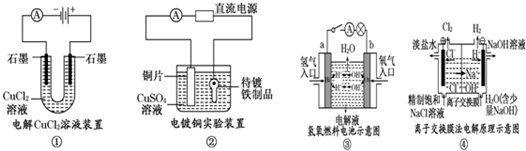

| A. | 装置①中阳极上析出红色固体 | |
| B. | 装置②的待镀铁制品应与电源负极相连 | |
| C. | 装置③中外电路电子由a极流向b极 | |
| D. | 装置④的阳极反应为:2H++2e-=H2↑ |
 .
.