题目内容
13.下列有关化学用语表达正确的是( )| A. | 氟化氢的电子式: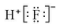 | |
| B. | 氯原子的结构示意图: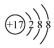 | |
| C. | 丙烯的结构简式:C3H6 | |
| D. | 硫原子的最外层电子排布式:3s23p4 |
分析 A.氟化氢共价化合物,不存在阴阳离子;
B.氯原子是17号元素,核外最外层电子数为7;
C.丙烯分子中含有碳碳双键;
D.硫原子最外层电子数为6,根据能量最低原理书写最外层电子排布式.
解答 解:A.氟化氢共价化合物,其电子式为 ,故A错误;
,故A错误;
B.氯原子是17号元素,核外电子分为三个电子层,原子结构示意图为 ,故B错误;
,故B错误;
C.丙烯的结构简式为CH2=CH-CH3,丙烯的分子式为C3H6,故C错误;
D.硫原子最外层电子数为6,电子排布式为3s23p4,故D正确.
故选:D.
点评 本题考查电子式、结构示意图、结构简式以及核外电子排布,比较基础,侧重对基础知识的巩固.

练习册系列答案
相关题目
3.食醋(主要成分CH3COOH)、纯碱(Na2CO3)和小苏打(NaHCO3)均为家庭厨房中常用的物质.己知:
请回答下列问题:
(1)25℃时,0.10mol•L-1Na2CO3溶液的pH=11,则溶液中由水电离出的c(OH-)=10-3
(2)常温下,将20mL0.10mol•L-1CH3COOH溶液和 20mL0.10mol•L-1HNO2 溶液分别与 20mL 0.10mol•L-1NaHCO3溶液混合(混合后溶液体积变化忽略不计).
①反应开始时,v (CH3COOH )<v (HNO2)(填“>”、“<”或“:”).
②充分反应后.两溶液中c(CH3COO-)< c(NO2-)(填“>”、“<”或“=”).
(3)25℃时,向CH3COOH溶液中加入一定量的NaHCO3,所得混合液的pH=6,则混合液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=18;
(4)常温下,下列方法可以使0.1mol•L-1CH3COOH的电离程度增大的是bc.
a.加入少量的稀盐酸
b.加热溶液
c.加水稀释
d.加入少量冰醋酸.
| 弱酸 | CH3COOH | H2CO3 | HNO2 |
| 电离常数 | K=1.8×10-5 | K=4.3×10-7 K=5.6×10-11 | K=5.0×10-4 |
(1)25℃时,0.10mol•L-1Na2CO3溶液的pH=11,则溶液中由水电离出的c(OH-)=10-3
(2)常温下,将20mL0.10mol•L-1CH3COOH溶液和 20mL0.10mol•L-1HNO2 溶液分别与 20mL 0.10mol•L-1NaHCO3溶液混合(混合后溶液体积变化忽略不计).
①反应开始时,v (CH3COOH )<v (HNO2)(填“>”、“<”或“:”).
②充分反应后.两溶液中c(CH3COO-)< c(NO2-)(填“>”、“<”或“=”).
(3)25℃时,向CH3COOH溶液中加入一定量的NaHCO3,所得混合液的pH=6,则混合液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=18;
(4)常温下,下列方法可以使0.1mol•L-1CH3COOH的电离程度增大的是bc.
a.加入少量的稀盐酸
b.加热溶液
c.加水稀释
d.加入少量冰醋酸.
4.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 100 mL 0.2 mol•L-1蔗糖溶液中所含分子总数为0.02NA | |
| B. | 40mL 10mol•L-1的浓盐酸与足量的MnO2充分反应,生成氯气的分子数为0.1NA | |
| C. | 标准状况下,22.4L CHCl3中含有的氯原子数目为3NA | |
| D. | 14g CO 和N2混合气体中含有的电子总数为7NA |
8.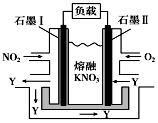 某燃料电池的工作原理如右图所示,该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用.下列说法正确的是( )
某燃料电池的工作原理如右图所示,该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用.下列说法正确的是( )
 某燃料电池的工作原理如右图所示,该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用.下列说法正确的是( )
某燃料电池的工作原理如右图所示,该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用.下列说法正确的是( )| A. | 该电池放电时K+向石墨Ⅰ电极迁移 | |
| B. | 石墨Ⅰ附近发生的反应:NO2-e-+NO3-═N2O5 | |
| C. | O2在石墨Ⅱ附近发生氧化反应,Y为NO | |
| D. | 相同条件下,放电过程中消耗的NO2和O2的体积比为2:1 |
18.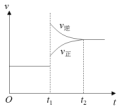 如图是工业合成氨反应的速率-时间图象,在 t1时刻改变某一条件,到 t2时重新达到平衡,判断 t1时刻可能改变条件是( )
如图是工业合成氨反应的速率-时间图象,在 t1时刻改变某一条件,到 t2时重新达到平衡,判断 t1时刻可能改变条件是( )
 如图是工业合成氨反应的速率-时间图象,在 t1时刻改变某一条件,到 t2时重新达到平衡,判断 t1时刻可能改变条件是( )
如图是工业合成氨反应的速率-时间图象,在 t1时刻改变某一条件,到 t2时重新达到平衡,判断 t1时刻可能改变条件是( )| A. | 使用催化剂 | B. | 升高温度 | C. | 增大压强 | D. | 提高 N2浓度 |
5.氮化硅(Si3N4)是一种新型的耐高温耐磨材料,氮化硅属于( )
| A. | 离子晶体 | B. | 分子晶体 | C. | 金属晶体 | D. | 原子晶体 |
2.实验室用如图所示的装置蒸馏海水,下列说法正确的是( )
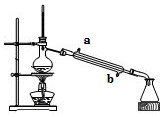

| A. | 蒸馏烧瓶中加入沸石的作用是防止暴沸 | |
| B. | 实验时冷却水应从a进入,从b流出 | |
| C. | 锥形瓶中能收集到高浓度的氯化钠溶液 | |
| D. | 该装置可用于分离海水中的NaCl和MgCl2 |
15. 在100℃时,将0.100mol的四氧化二氨气体充入1L恒容抽空的密闭容器中,隔一定时间对该容器内的物质浓度进行分析得到表数据:
在100℃时,将0.100mol的四氧化二氨气体充入1L恒容抽空的密闭容器中,隔一定时间对该容器内的物质浓度进行分析得到表数据:
(1)该反应的平衡常数表达式为$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$;从表中数据分析:c1<c2;(填“>”“<”或“=”).
(2)在图中画出并标明此反应中N2O4和NO2的浓度随时间变化的曲线.
(3)在上述条件下,从反应开始至达到化学平衡时,四氧化二氮的平均反应速率为0.001mol•L-1•s-1.
(4)随温度升高,混合气体的颜色变深,反应的△H>0(填“大于”“小于”)
(5)达平衡后下列条件的改变可使NO2气体浓度增大的是B.
A.增大容器的容积B.再充入一定量的N2O4C.分离出一定量的NO2D.再充入一定量的He
(6)若起始时充入NO2气体0.080mol,N2O4气体0.010mol,通过计算判断反应进行的方向.
 在100℃时,将0.100mol的四氧化二氨气体充入1L恒容抽空的密闭容器中,隔一定时间对该容器内的物质浓度进行分析得到表数据:
在100℃时,将0.100mol的四氧化二氨气体充入1L恒容抽空的密闭容器中,隔一定时间对该容器内的物质浓度进行分析得到表数据:| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| c(N2O4)/mol•L-1 | 0.100 | c1 | 0.050 | 0.040 | 0.040 |
| c(NO2)/mol•L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
(2)在图中画出并标明此反应中N2O4和NO2的浓度随时间变化的曲线.
(3)在上述条件下,从反应开始至达到化学平衡时,四氧化二氮的平均反应速率为0.001mol•L-1•s-1.
(4)随温度升高,混合气体的颜色变深,反应的△H>0(填“大于”“小于”)
(5)达平衡后下列条件的改变可使NO2气体浓度增大的是B.
A.增大容器的容积B.再充入一定量的N2O4C.分离出一定量的NO2D.再充入一定量的He
(6)若起始时充入NO2气体0.080mol,N2O4气体0.010mol,通过计算判断反应进行的方向.