题目内容
乙酸环己酯具有香蕉及苹果的气味,主要用于配制各种饮料、冰淇淋等,实验室制备乙酸环己酯的反应原理、装置示意图1和有关数据如下:

实验步骤:
将12.0g(0.2mol)乙酸、l0.0g(0.1mol)环己醇和15mL环己烷加入装有温度计、恒压滴液漏斗和球形冷凝管的四颈烧瓶中,在搅拌下,慢慢滴加15mL 98%浓硫酸,滴加完后将恒压滴液漏斗换成分水器装置(如图2),加热回流90min后,向反应液中依次加入水、10%的NaHCO3溶液、水洗涤,然后加入无水MgSO4,放置过夜,加热蒸馏,收集168-174℃的馏分,得到无色透明、有香味的液体产品6.9g
(1)上述反应装置图中存在的一处错误是 .
(2)实验中控制乙酸的物质的量是环己醇的2倍,其目的是 .
(3)使用分水器的目的是 .
(4)用l0%的NaHCO3溶液洗涤的目的是 ;第二次水洗的目的是 ;加人无水MgSO4的目的是 .
(5)本次实验的产率为 .
(6)在进行蒸馏操作时,若采用如图3装置,会使实验的产率 (填“偏高”或“偏低”),其原因是 .

 | 相对分子质量 | 密度/g?cm-3[来源:.Com] | 沸点 | 水中溶解性 | |
| 乙酸 | 60 | 1.051 | 118.0 | 溶 | |
| 环己醇 | 100 | 0.982 | 160.8 | 微溶 | |
| 乙酸环己酯 | 142 | 0.969 | 173.5 | 难溶 |
将12.0g(0.2mol)乙酸、l0.0g(0.1mol)环己醇和15mL环己烷加入装有温度计、恒压滴液漏斗和球形冷凝管的四颈烧瓶中,在搅拌下,慢慢滴加15mL 98%浓硫酸,滴加完后将恒压滴液漏斗换成分水器装置(如图2),加热回流90min后,向反应液中依次加入水、10%的NaHCO3溶液、水洗涤,然后加入无水MgSO4,放置过夜,加热蒸馏,收集168-174℃的馏分,得到无色透明、有香味的液体产品6.9g
(1)上述反应装置图中存在的一处错误是
(2)实验中控制乙酸的物质的量是环己醇的2倍,其目的是
(3)使用分水器的目的是
(4)用l0%的NaHCO3溶液洗涤的目的是
(5)本次实验的产率为
(6)在进行蒸馏操作时,若采用如图3装置,会使实验的产率
考点:物质分离、提纯的实验方案设计,有机物的合成,制备实验方案的设计
专题:实验题
分析:(1)根据装置中仪器的使用方法判断;
(2)酯化反应是可逆反应,增加一种反应物的物质的量可以提高另一种反应物的转化率;
(3)减少生成的物质的量可以提高反应物的转化率;
(4)反应液中有硫酸、醋酸等酸性物质,可以与碳酸氢钠反应,再用水除去碳酸氢钠;无水MgSO4的具有吸水性;
(5)根据产率=
×100%进行计算;
(6)环己醇的沸点比乙酸环己酯低,若采用如图3装置,产品中有未反应的环己醇.
(2)酯化反应是可逆反应,增加一种反应物的物质的量可以提高另一种反应物的转化率;
(3)减少生成的物质的量可以提高反应物的转化率;
(4)反应液中有硫酸、醋酸等酸性物质,可以与碳酸氢钠反应,再用水除去碳酸氢钠;无水MgSO4的具有吸水性;
(5)根据产率=
| 实际产量 |
| 理论产量 |
(6)环己醇的沸点比乙酸环己酯低,若采用如图3装置,产品中有未反应的环己醇.
解答:
解:(1)冷凝管使用时,冷凝水应从下口进上口出,
故答案为:冷凝水应从下口进上口出;
(2)酯化反应是可逆反应,增加一种反应物的物质的量可以提高另一种反应物的转化率,所以增加乙酸的量可以提高环已醇的转化率,
故答案为:提高环已醇的转化率;
(3)在制乙酸环己酯的反应中,水是生成物,将生成的水及时从体系中分离出来,提高反应物的转化率,
故答案为:将生成的水及时从体系中分离出来,提高反应物的转化率;
(4)反应混合液中有硫酸、醋酸等酸性物质,可以与碳酸氢钠反应,所以可以用再用碳酸氢钠洗去硫酸和醋酸,再用水可以洗去碳酸氢钠,无水MgSO4的具有吸水性,所以用,无水MgSO4干燥产品,
故答案为:洗去硫酸和醋酸;洗去碳酸氢钠;干燥;
(5)0.2mol乙酸和0.1mol环己醇反应,理论上可以生成0.1mol乙酸环己酯,即14.2g,而实际产量是6.9g,所以本次实验的产率=
×100%=
×100%=48.6%,
故答案为:48.6%;
(6)环己醇的沸点比乙酸环己酯低,若采用如图3装置,产品中有未反应的环己醇,所以会使实验的产率偏高,
故答案为:偏高;产品中会收集到未反应的环己醇.
故答案为:冷凝水应从下口进上口出;
(2)酯化反应是可逆反应,增加一种反应物的物质的量可以提高另一种反应物的转化率,所以增加乙酸的量可以提高环已醇的转化率,
故答案为:提高环已醇的转化率;
(3)在制乙酸环己酯的反应中,水是生成物,将生成的水及时从体系中分离出来,提高反应物的转化率,
故答案为:将生成的水及时从体系中分离出来,提高反应物的转化率;
(4)反应混合液中有硫酸、醋酸等酸性物质,可以与碳酸氢钠反应,所以可以用再用碳酸氢钠洗去硫酸和醋酸,再用水可以洗去碳酸氢钠,无水MgSO4的具有吸水性,所以用,无水MgSO4干燥产品,
故答案为:洗去硫酸和醋酸;洗去碳酸氢钠;干燥;
(5)0.2mol乙酸和0.1mol环己醇反应,理论上可以生成0.1mol乙酸环己酯,即14.2g,而实际产量是6.9g,所以本次实验的产率=
| 实际产量 |
| 理论产量 |
| 6.9g |
| 14.2g |
故答案为:48.6%;
(6)环己醇的沸点比乙酸环己酯低,若采用如图3装置,产品中有未反应的环己醇,所以会使实验的产率偏高,
故答案为:偏高;产品中会收集到未反应的环己醇.
点评:考查了常见仪器的构造与安装、混合物的分离、提纯、物质的制取、药品的选择及使用、物质产率的计算等知识,题目难度中等,试题涉及的题量较大,知识点较多,充分培养了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
测得室温下0.1mol?L-1的某酸HA溶液的PH=3,下列叙述错误的是( )
| A、HA是弱酸 |
| B、若升高温度,溶液的PH增大 |
| C、此酸的电离平衡常数约为10-5 |
| D、由HA电离出的c(H+)约为水电离出的c(H+)的108倍 |
“绿色化学”要求不产生副产物,实现零排放.现实验室中要合成一溴乙烷,下列最符合绿色化学要求的是( )
| A、乙烷和溴蒸气在光照下发生反应 |
| B、将乙烯通入溴水中发生反应 |
| C、乙烯与溴化氢在一定条件下反应 |
| D、乙炔与溴化氢在一定条件下反应 |
我国新报道的高温超导材料中,铊(Tl)是其中重要的组成成分之一.已知与铝同主族,位于元素周期表的第六周期.则下列关于铊的叙述中,可能有错误的是( )
| A、铊元素的原子半径大于铝元素的原子半径 |
| B、铊单质的固体硬度较小 |
| C、铊的最高氧化物对应的水化物为Tl(OH)3 |
| D、铊及其化合物都没有毒性 |
下列各物质的溶液不能与二氧化碳反应的是( )
| A、氯化铝 | B、偏铝酸钠 |
| C、硅酸钠 | D、碳酸钠 |
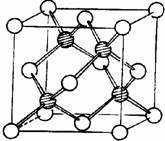 冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图,其中空心球所示原子位于立方体的顶点或面心,实心球所示原子位于立方体内)类似.每个冰晶胞平均占有
冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图,其中空心球所示原子位于立方体的顶点或面心,实心球所示原子位于立方体内)类似.每个冰晶胞平均占有