题目内容
|
在t℃时,某Ba(OH)2的稀溶液中c(H+)=10-a mol/L,c(OH-)=10-b mol/L,已知a+b=12.向该溶液中逐滴加入pH=c的盐酸,测得混合溶液的部分pH如下表所示.
假设溶液混合前后体积变化忽略不计,则c为 | |
| [ ] | |
A. |
3 |
B. |
4 |
C. |
5 |
D. |
6 |
解析:
|
本题考查的是电解质溶液的混合计算.由题意知,在t℃时,水的离子积常数为10-12.所以溶液呈中性时的pH=6,由①可知Ba(OH)2溶液的浓度为10-4 mol/L,再结合③可知两者正好反应,所以盐酸的浓度也为10-4 mol/L,pH=4. |

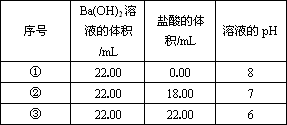
序号 | Ba(OH)2溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
① | 22.00 | 0.00 | 8 |
② | 22.00 | 18.00 | 7 |
③ | 22.00 | 22.00 | 6 |
假设溶液混合前后体积变化忽略不计,则c为
A.3 B
在t℃时,某Ba(OH)2的稀溶液中c(H+)=10-a mol/L,c(OH-)=10-b mol/L,已知a+b=12。向该溶液中逐滴加入pH=c的盐酸,测得混合溶液的部分pH如下表所示:
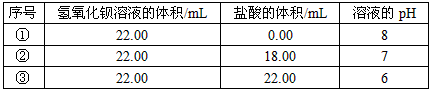
| 序号 | 氢氧化钡溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |
A.3 B.4 C.5 D.6
(山东省平度一中测试)在t℃时,某Ba(OH)2的稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12。向该溶液中逐滴加入pH=c的盐酸,测得混合溶液的部分pH如下表所示。
序号 | Ba(OH)2溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
① | 22.00 | 0.00 | 8 |
② | 22.00 | 18.00 | 7 |
③ | 22.00 | 22.00 | 6 |
假设溶液混合前后体积变化忽略不计,则c为 ( )
A.3 B.4 C.5 D.6
在t℃时,某Ba(OH)2的稀溶液中C(H+)=10-amol/L, C(OH¯)=10-bmol/L,已知a+b=12。
向该溶液中逐滴加入pH=c的盐酸,测得混合溶液的部分pH如下表所示。
| 序号 | Ba(OH)2溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |
假设溶液混合前后体积变化忽略不计,则c为( )
A. 3 B.4 C.5 D.6