题目内容
氯元素构成的双原子分子有三种,其相对分子质量分别为70、72、74,此三种分子个数之比为6:3:1.下列说法正确的是( )
| A、氯元素有三种同位素 |
| B、必存在质量数为36的同位素 |
| C、氯气分子的平均相对质量为72 |
| D、质量数最小的氯元素所占原子百分数为百分之75 |
考点:同位素及其应用
专题:原子组成与结构专题
分析:氯元素所形成的气态双原子分子有三种,说明氯元素有两种同位素,根据三种分子的相对分子质量可知,原子的相对原子质量分别为35、37,72是两种同位素形成的分子式量,根据三种分子物质的量之比求的各同位素所占的原子百分比;三种分子的平均式量可根据平均摩尔质量的定义求出.
解答:
解:A.根据题意氯原子的相对质量只能有2种,即35、37,若有3种或更多,则形成的双原子分子的式量就不止3种,故A错误;
B.两种同位素原子构成三种分子,质量数应为35、37,三种分子组成为35Cl2 、37Cl2,35Cl37Cl,故B错误;
C.Cl2的平均式量=总质量/总物质的量=(6×70+3×72+1×74)÷(6+3+1)=71,故C错误;
D.三种分子组成为35Cl2 、35Cl37Cl、37Cl2,按照物质的量之比为6:3:1,则35Cl和37Cl的物质的量之比(6×2+3):(3+1×2)=15:5=3:1,质量数35的同位素原子百分比为75%,故D正确;
故选D.
B.两种同位素原子构成三种分子,质量数应为35、37,三种分子组成为35Cl2 、37Cl2,35Cl37Cl,故B错误;
C.Cl2的平均式量=总质量/总物质的量=(6×70+3×72+1×74)÷(6+3+1)=71,故C错误;
D.三种分子组成为35Cl2 、35Cl37Cl、37Cl2,按照物质的量之比为6:3:1,则35Cl和37Cl的物质的量之比(6×2+3):(3+1×2)=15:5=3:1,质量数35的同位素原子百分比为75%,故D正确;
故选D.
点评:本题考查元素同位素的含义和应用,难度不大,注意平均式量=总质量/总物质的量.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
下列实验操作中,正确的是( )
| A、为使过滤速率加快,可用玻璃棒在过滤器中轻轻搅拌,加速液体流动 |
| B、用酒精灯给试管加热时,要将被加热的试管放在酒精灯火焰的外焰上 |
| C、为加速固体物质的溶解只能采用加热的方法 |
| D、为增大气体物质的溶解度,常采取搅拌、加热等措施 |
 盆烯是近年合成的一种有机物,它的分子结构可简化表示为(其中C、H原子已略去),下列关于盆烯的说法中错误的是( )
盆烯是近年合成的一种有机物,它的分子结构可简化表示为(其中C、H原子已略去),下列关于盆烯的说法中错误的是( )| A、盆烯是乙烯的一种同系物 |
| B、盆烯分子中所有的碳原子不可能在同一平面上 |
| C、盆烯是苯的一种同分异构体 |
| D、盆烯在一定条件下可以发生加成反应 |
下列变化过程中,需要加入氧化剂的是( )
| A、HCl→H2 |
| B、HCl→FeCl2 |
| C、H2SO4→SO2 |
| D、Fe→Fe2O3 |
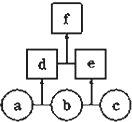 如图所示,a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,且分子中所含原子个数:d>e,f为离子化合物.则下列说法错误的是( )
如图所示,a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,且分子中所含原子个数:d>e,f为离子化合物.则下列说法错误的是( )| A、常温下,单质a呈气态 |
| B、单质c具有强氧化性 |
| C、稳定性:d>e |
| D、f受热易分解为d和e |