题目内容
下列离子方程式表达正确的( )
| A、硫化钠的水解反应:S2-+2H2O?H2S+2OH- |
| B、铝片跟氢氧化钠溶液反应:Al+2OH-═AlO2-+H2 |
| C、在硫酸亚铁溶液中通入氧气:4Fe2++O2+4H+═4Fe3++2OH- |
| D、向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O═HClO+HSO3- |
考点:离子方程式的书写
专题:离子反应专题
分析:A、硫离子水解分步进行,主要以第一步为主;
B、根据电子守恒或电荷守恒判断,离子方程式两边电子和电荷都不守恒;
C、亚铁离子具有还原性,能够被氧气氧化成铁离子;
D、次氯酸具有强氧化性,能够将二氧化硫氧化成硫酸根离子.
B、根据电子守恒或电荷守恒判断,离子方程式两边电子和电荷都不守恒;
C、亚铁离子具有还原性,能够被氧气氧化成铁离子;
D、次氯酸具有强氧化性,能够将二氧化硫氧化成硫酸根离子.
解答:
解:A、硫化钠的水解反应主要以第一步为主,其电离方程式为:S2-+H2O?HS-+OH-,故A错误;
B、铝片跟氢氧化钠溶液反应的离子方程式为:2Al+2H2O+2OH-═2AlO2-+3H2↑,故B错误;
C、在硫酸亚铁溶液中通入氧气,亚铁离子被氧气氧化,反应的离子方程式为:4Fe2++O2+4H+═4Fe3++2OH-,故C正确;
D、向次氯酸钠溶液中通入足量SO2气体,二氧化硫被氧化成硫酸根离子,反应的离子方程式为:SO2+ClO-+H2O═SO42-+2H++Cl-,故D错误;
故选:C.
B、铝片跟氢氧化钠溶液反应的离子方程式为:2Al+2H2O+2OH-═2AlO2-+3H2↑,故B错误;
C、在硫酸亚铁溶液中通入氧气,亚铁离子被氧气氧化,反应的离子方程式为:4Fe2++O2+4H+═4Fe3++2OH-,故C正确;
D、向次氯酸钠溶液中通入足量SO2气体,二氧化硫被氧化成硫酸根离子,反应的离子方程式为:SO2+ClO-+H2O═SO42-+2H++Cl-,故D错误;
故选:C.
点评:本题考查了离子方程式的书写判断,该题是高考中的高频题,侧重对学生能力的培养和训练,该题需要明确判断离子方程式常用方法:(1)检查反应能否发生;(2)检查反应物、生成物是否正确;(3)检查各物质拆分是否正确;(4)检查是否符合守恒关系(如:质量守恒和电荷守恒等);(5)检查是否符合原化学方程式,然后灵活运用即可.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A、铁、铜和稀硫酸构成原电池,当转移了NA个电子时,产生的气体体积一定为11.2L |
| B、常温下,1L 0.1mol?L-1氯化镁溶液中,阳离子总数小于0.1NA |
| C、常温常压下,56g氮气与一氧化碳的混合气体中所含原子数目为4NA |
| D、在标准状况下,2.24L的乙烷中含有共价键的数目为0.6NA |
设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、标准状况下,11.2L CCl4含有的分子数目为0.5NA |
| B、在常温常压下,1mol氦气所含原子数为2NA |
| C、10g重水(D2O)里含有的电子数为10NA |
| D、标准状况下,22.4L NO2气体含有的分子数目小于NA |
14C是碳的一种同位素,NA为阿伏加德罗常数,下列说法中不正确的是( )
①1mol 14CH4分子中所含中子数为8NA
②7g 14C原子形成的石墨中所含质子数为3NA
③17g甲基(-14CH3)所含电子数为8NA
④常温常压下,22.4L 14CO2其分子数为NA.
①1mol 14CH4分子中所含中子数为8NA
②7g 14C原子形成的石墨中所含质子数为3NA
③17g甲基(-14CH3)所含电子数为8NA
④常温常压下,22.4L 14CO2其分子数为NA.
| A、①② | B、①③ | C、①②③ | D、③④ |
下列说法正确的是( )
| A、pH=0的溶液中能大量共存:NO3-、SO42-、Na+、I- |
| B、0.1mol?L-1 Na2S溶液中:c(Na+)>2c(S2-) |
| C、NaHSO3溶液中 c(HSO3-)+c(OH-)+c(SO32-)=c(H+)+c(Na+) |
| D、等体积的硝酸和氨水混合可能存在:c(NO3-)=c(NH4+) |
NA为阿伏伽德罗常数的值,下列叙述中正确的是( )
| A、1L 1mol?L-1的氯化铁溶液中Fe3+的数目为NA |
| B、标准状况下,2.24LCl2含有的分子数为0.1NA |
| C、78g Na2O2固体与足量H2O反应转移的电子数为NA |
| D、t℃时,1L pH=6的纯水中OH-的数目为10-8NA |
能在无色水溶液中大量共存的一组离子是( )
| A、H+、Fe3+、I-、Cl- |
| B、Al3+、Mg2+、NO3-、Cl- |
| C、K+、Ag+、Ca2+、PO43- |
| D、NH4+、Na+、AlO2-、MnO4- |
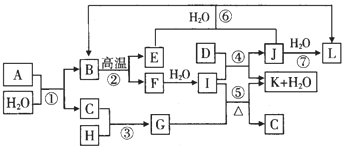
 W、Q、R、X、Y、Z六种原子序数依次递增的主族元素.已知W、Y的单质在常温下是气体;QW4分子在一定条件下与Y的单质连续反应,共生成五种产物;R与Y、Z与Y均可形成离子个数比为1:1的晶体,在这两种晶体中,每个Y离子吸引的R离子与Z离子的个数比为3:4.X的单质一定条件下能在Q的最高价氧化物中剧烈燃烧.请回答下列问题:
W、Q、R、X、Y、Z六种原子序数依次递增的主族元素.已知W、Y的单质在常温下是气体;QW4分子在一定条件下与Y的单质连续反应,共生成五种产物;R与Y、Z与Y均可形成离子个数比为1:1的晶体,在这两种晶体中,每个Y离子吸引的R离子与Z离子的个数比为3:4.X的单质一定条件下能在Q的最高价氧化物中剧烈燃烧.请回答下列问题: