��Ŀ����
5��һ���¶����У�a�����ᡡb�����ᡡc�����������ᣮ��1���������ʵ���Ũ����ͬʱ��c��H+���ɴ�С��˳����b��a��c��
��2��ͬ�����ͬ���ʵ���Ũ�ȵ������ᣬ�к�NaOH������˳����b��a=c��
��3����c��H+����ͬ�������ͬʱ��ͬʱ����п����������ͬ�����H2����ͬ״��������ʼʱ�ķ�Ӧ����a=b=c����Ӧ����ʱ��c��a=b��
��4����c��H+����ͬ���������ϡ��10����c��H+���ɴ�С��˳����c��a=b��
���� ��1������Ϊ��Ԫ�ᣬ����Ϊǿ�ᣬ����Ϊ���
��2��ͬ���ͬ���ʵ���Ũ�ȵ������ᣬ�������������ʵ�����ȣ�������Ϊ��Ԫ�
��3����Ӧ������������Ũ���йأ�������Ũ����ͬ����Ӧ������ͬ�����ڴ����ڷ�Ӧ�����е���̶������������п��Ӧ��ƽ���������
��4������Ϊ���ᣬϡ�����д���ĵ���̶�������ϡ�ͺ������������Ũ����������������Һ��������Ũ����ȣ�
��� �⣺��1������Ϊ��Ԫ�ᣬ����Ϊǿ�ᣬ����Ϊ���ᣬ�����ʵ���Ũ����ͬʱ��c��H+���ɴ�С��˳����b��a��c��
�ʴ�Ϊ��b��a��c��
��2��ͬ���ͬ���ʵ���Ũ�ȵ������ᣬ�������������ʵ�����ȣ�������Ϊ��Ԫ�ᣬ���к�ͬ���ʵ���Ũ�ȵ�NaOH���ĵ�����ɴ�С��˳���ǣ�b��a=c��
�ʴ�Ϊ��b��a=c��
��3����c��H+����ͬ�������ͬʱ����ʼʱ��Ӧ������ͬ������a=b=c��
������ȫ���룬ֻ�д����ڼ������룬�������п��Ӧ��ƽ��������죬�����������п�ķ�Ӧ������ȣ����Էֱ��������п��������ͬ�����H2����ͬ״������Ӧ����ʱ�䣺c��a=b��
�ʴ�Ϊ��a=b=c��c��a=b��
��4����c��H+����ͬ���������ϡ��10������ĵ���̶������������ϡ�ͺ�������Ũ����������HCl����ǿ����ʣ�ϡ�ͺ���ߵ�c��H+����ȣ�����ϡ�ͺ�������Ũ���ɴ�С��˳���ǣ�c��a=b��
�ʴ�Ϊ��c��a=b��
���� ���⿼��������ʵĵ���ƽ�⡢��ѧ��Ӧ���ʵ�Ӱ�����ص�֪ʶ����Ŀ�Ѷ��еȣ�ע������Ӱ�컯ѧ��Ӧ���ʡ�����ƽ������أ���ȷ������ʲ��ֵ�����ص㣬����������ѧ���ķ������������Ӧ��������

��1���Ʊ��ϳɰ�ԭ����H2�����ü�������ת��������Ҫת����Ӧ���£�
CH4��g��+H2O��g��?CO��g��+3H2��g����H=+206.2kJ/mol
CH4��g��+2H2O��g��?CO2��g��+4H2��g����H=+165.0kJ/mol
������Ӧ����ԭ�����е�CO��ʹ���ϳɴ����ж��������ȥ����ҵ�ϳ����ô���������CO��ˮ������Ӧ�����׳�ȥ��CO2��ͬʱ�ֿ��Ƶõ�����������ķ������˷�Ӧ��Ϊһ����̼�任��Ӧ���÷�Ӧ���Ȼ�ѧ����ʽ��CO��g��+H2O��g��?CO2��g��+H2��g����H=-41.2 kJ/mol��
��2����ҵ�������ص�ԭ������NH3��CO2Ϊԭ�Ϻϳ�����[CO��NH2��2]����Ӧ�Ļ�ѧ����ʽΪ��2NH3 ��g��+CO2 ��g��?CO��NH2��2 ��l��+H2O ��l�����÷�Ӧ��ƽ�ⳣ�����¶ȹ�ϵ���£�
| T/�� | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
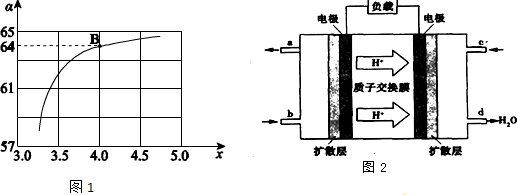
����һ���¶Ⱥ�ѹǿ�£���ԭ�����е�NH3��CO2�����ʵ���֮�ȣ���̼�ȣ�$\frac{n��N{H}_{3}��}{n��C{O}_{2}��}$=x����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ����ͼ1�е�B�㴦��NH3��ƽ��ת����32%��
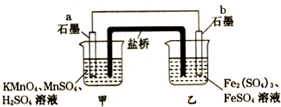
��3����֪����ȼ�ϵ�صĹ���ԭ����ͼ2��ʾ���õ�ع���ʱ��a�ڷų�������ΪCO2���õ�������ĵ缫��ӦʽΪ��O2+4e-+4H+=2H2O������һ��ʱ���3.2g������ȫ��Ӧ����CO2ʱ����1.6mol ���ӷ���ת�ƣ�
��Pb+2Cl2�TPbCl4��Sn+2Cl2�TSnCl4��SnCl2+Cl2�TSnCl4
��PbO2+4HCl�TPbCl4+2H2O��Pb3O4+8HCl�T3PbCl2+Cl2��+4H2O��
| A�� | �ڢۢ� | B�� | �ڢۢ� | C�� | �٢ڢ� | D�� | �٢ڢܢ� |
| A�� | SO${\;}_{4}^{2-}$ | B�� | CO${\;}_{3}^{2-}$ | C�� | Al3+ | D�� | NO3- |
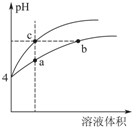
 �����ͼԭ��أ�2KMnO4+10FeSO4+8H2SO4�T2MnSO4+5Fe2��SO4��3+K2SO4+8H2O����������װ�б�����Һ������˵����ȷ���ǣ�������
�����ͼԭ��أ�2KMnO4+10FeSO4+8H2SO4�T2MnSO4+5Fe2��SO4��3+K2SO4+8H2O����������װ�б�����Һ������˵����ȷ���ǣ�������| A�� | ���·���ӵ������Ǵ�a��b | |
| B�� | ��ع���ʱ�������е�SO42-������ձ� | |
| C�� | a�缫�Ϸ����ķ�ӦΪ��MnO4-+8H++5e-�TMn2++4H2O | |
| D�� | ˫Һԭ��ع���ʱ�������������� |
 Ϊ��֤��һˮ�ϰ���NH3•H2O����������ʣ��ס��Ҷ��˷ֱ�ѡ�������Լ�����ʵ�飺��ˮ��0.10mol•L-1NH4Cl��Һ��NH4Cl���塢��̪��Һ��pH��ֽ������ˮ��
Ϊ��֤��һˮ�ϰ���NH3•H2O����������ʣ��ס��Ҷ��˷ֱ�ѡ�������Լ�����ʵ�飺��ˮ��0.10mol•L-1NH4Cl��Һ��NH4Cl���塢��̪��Һ��pH��ֽ������ˮ��