题目内容
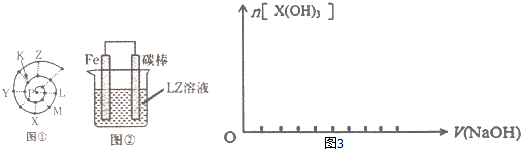
某小组在研究前18号元素时发现:依据不同的标准和规律,元素周期表有不同的排列形式.如果将它们按原子序数递增的顺序排列,可形成图①所示的“蜗牛”形状,图中每个“.”代表一种元素,其中P点代表氢元素.
(1)X元素在常规周期表中的位置 (填周期和族).
(2)写出M与Z两种元素形成的化合物的电子式 .
(3)下列说法正确的是 .
a.Z元素对应的氢化物比K元素对应的氢化物沸点高
b.虚线相连的元素处于同一主族
c.K、L、X三种元素的离子半径大小顺序是X3+>L+>K2-
d.由K、L两种元素组成的化合物中可能含有共价键
(4)图②装置可以模拟钢铁的腐蚀,铁棒一极的电极反应式是 .若在图②溶液中滴加少量酚酞溶液并进行电解,发现Fe电极附近溶液变红,写出该电解池的离子方程式 .
牺牲阳极的阴极保护法利用的是 原理(填“电解池”或“原电池”).
(5)已知室温下,X(OH)3的Ksp或溶解度远大于Fe(OH)3.向浓度均为0.01mol?L-1的Fe(NO3)3和X(NO3)3混合溶液中,逐滴加入NaOH溶液.请在下列坐标不意图中画出生成X(OH)3的物质的量与加入NaOH溶液的体积的关系
(1)X元素在常规周期表中的位置
(2)写出M与Z两种元素形成的化合物的电子式
(3)下列说法正确的是
a.Z元素对应的氢化物比K元素对应的氢化物沸点高
b.虚线相连的元素处于同一主族
c.K、L、X三种元素的离子半径大小顺序是X3+>L+>K2-
d.由K、L两种元素组成的化合物中可能含有共价键
(4)图②装置可以模拟钢铁的腐蚀,铁棒一极的电极反应式是
牺牲阳极的阴极保护法利用的是
(5)已知室温下,X(OH)3的Ksp或溶解度远大于Fe(OH)3.向浓度均为0.01mol?L-1的Fe(NO3)3和X(NO3)3混合溶液中,逐滴加入NaOH溶液.请在下列坐标不意图中画出生成X(OH)3的物质的量与加入NaOH溶液的体积的关系

考点:位置结构性质的相互关系应用,化学电源新型电池
专题:
分析:(1)X元素是Al元素,据此判断Al元素在周期表中的位置;
(2)M是Mg元素、Z是Cl元素,二者通过得失电子生成离子化合物氯化镁;
(3)a.K为O元素,Z为F元素,其氢化物分子间形成的氢键数目越多,沸点越高;
b.虚线相连的元素处于同一族;
c.电子层数越多其离子半径越大,电子层结构相同的离子,离子半径随着原子序数增大而减小;
d.由K、L两种元素组成的化合物可能是Na2O或Na2O2,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键;
(4)L是Na、Z是Cl元素,LZ溶液是NaCl溶液,中性条件下,铁发生吸氧腐蚀,Fe作负极、C作正极,负极上Fe失电子发生氧化反应,若在图②溶液中滴加少量酚酞溶液并进行电解,发现Fe电极附近溶液变红,则Fe作阴极、C作阳极,电解氯化钠溶液得到氢氧化钠、氯气和氢气,牺牲阳极的阴极保护法利用的原理是原电池原理;
(5)室温下,Al(OH)3的Ksp或溶解度远大于Fe(OH)3,向浓度均为0.1mol?L?1的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液,NaOH先和Fe(NO3)3反应生成Fe(OH)3,当铁离子完全反应后,Al(NO3)3再和NaOH反应生成Al(OH)3沉淀,但Al元素完全以Al(OH)3形式存在时,如果继续滴加NaOH溶液,Al(OH)3转化为NaAlO2而消失,据此画出图象.
(2)M是Mg元素、Z是Cl元素,二者通过得失电子生成离子化合物氯化镁;
(3)a.K为O元素,Z为F元素,其氢化物分子间形成的氢键数目越多,沸点越高;
b.虚线相连的元素处于同一族;
c.电子层数越多其离子半径越大,电子层结构相同的离子,离子半径随着原子序数增大而减小;
d.由K、L两种元素组成的化合物可能是Na2O或Na2O2,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键;
(4)L是Na、Z是Cl元素,LZ溶液是NaCl溶液,中性条件下,铁发生吸氧腐蚀,Fe作负极、C作正极,负极上Fe失电子发生氧化反应,若在图②溶液中滴加少量酚酞溶液并进行电解,发现Fe电极附近溶液变红,则Fe作阴极、C作阳极,电解氯化钠溶液得到氢氧化钠、氯气和氢气,牺牲阳极的阴极保护法利用的原理是原电池原理;
(5)室温下,Al(OH)3的Ksp或溶解度远大于Fe(OH)3,向浓度均为0.1mol?L?1的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液,NaOH先和Fe(NO3)3反应生成Fe(OH)3,当铁离子完全反应后,Al(NO3)3再和NaOH反应生成Al(OH)3沉淀,但Al元素完全以Al(OH)3形式存在时,如果继续滴加NaOH溶液,Al(OH)3转化为NaAlO2而消失,据此画出图象.
解答:
解:(1)X元素是Al元素,Al原子核外有3个电子层、最外层电子数是3,主族元素原子电子层数与其周期数相等、最外层电子数与其族序数相等,所以Al元素位于第三周期第IIIA族,故答案为:第三周期第IIIA族;
(2)M是Mg元素、Z是Cl元素,二者通过得失电子生成离子化合物氯化镁,其电子式为 ,故答案为:
,故答案为: ;
;
(3)a.K为O元素,Z为F元素,水、氟化氢分子间均有氢键,但是水分子间形成的氢键数目多余HF分子间形成的氢键数目,其氢化物分子间形成的氢键数目越多,沸点越高,所以水的沸点大于氟化氢,故错误;
b.虚线相连的元素处于同一族,图中包含主族和零族元素,不全部是主族,故错误;
c.电子层数越多其离子半径越大,电子层结构相同的离子,离子半径随着原子序数增大而减小,所以离子半径从小到大顺序为X3+<L+<K2?,故错误;
d.由K、L两种元素组成的化合物可能是Na2O或Na2O2,过氧化钠中存在离子键和共价键,故正确;
故答案为:d;
(4)L是Na、Z是Cl元素,LZ溶液是NaCl溶液,中性条件下,铁发生吸氧腐蚀,Fe作负极、C作正极,负极上Fe失电子发生氧化反应,电极反应式为Fe-2e-=Fe2+,若在图②溶液中滴加少量酚酞溶液并进行电解,发现Fe电极附近溶液变红,则Fe作阴极、C作阳极,电解氯化钠溶液得到氢氧化钠、氯气和氢气,电解方程式为:2Cl-+2H2O
H2↑+Cl2↑+2OH-,牺牲阳极的阴极保护法利用的原理是原电池原理,
故答案为:Fe-2e-=Fe2+;2Cl-+2H2O
H2↑+Cl2↑+2OH-;原电池;
(5)室温下,Al(OH)3的Ksp或溶解度远大于Fe(OH)3,向浓度均为0.1mol?L?1的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液,NaOH先和Fe(NO3)3反应生成Fe(OH)3,当铁离子完全反应后,Al(NO3)3再和NaOH反应生成Al(OH)3沉淀,但Al元素完全以Al(OH)3形式存在时,如果继续滴加NaOH溶液,Al(OH)3转化为NaAlO2而消失,所以滴加NaOH开始时没有氢氧化铝沉淀生成,当铁离子完全沉淀后再生成氢氧化铝沉淀,最后氢氧化铝完全溶解生成偏铝酸钠,因为硝酸铁和硝酸铝的浓度相等,则开始时不产生沉淀、生成氢氧化铝沉淀、氢氧化铝沉淀完全溶解需要NaOH的体积之比为3:3:1,所以其图象为 ,故答案为:
,故答案为: .
.
(2)M是Mg元素、Z是Cl元素,二者通过得失电子生成离子化合物氯化镁,其电子式为
 ,故答案为:
,故答案为: ;
;(3)a.K为O元素,Z为F元素,水、氟化氢分子间均有氢键,但是水分子间形成的氢键数目多余HF分子间形成的氢键数目,其氢化物分子间形成的氢键数目越多,沸点越高,所以水的沸点大于氟化氢,故错误;
b.虚线相连的元素处于同一族,图中包含主族和零族元素,不全部是主族,故错误;
c.电子层数越多其离子半径越大,电子层结构相同的离子,离子半径随着原子序数增大而减小,所以离子半径从小到大顺序为X3+<L+<K2?,故错误;
d.由K、L两种元素组成的化合物可能是Na2O或Na2O2,过氧化钠中存在离子键和共价键,故正确;
故答案为:d;
(4)L是Na、Z是Cl元素,LZ溶液是NaCl溶液,中性条件下,铁发生吸氧腐蚀,Fe作负极、C作正极,负极上Fe失电子发生氧化反应,电极反应式为Fe-2e-=Fe2+,若在图②溶液中滴加少量酚酞溶液并进行电解,发现Fe电极附近溶液变红,则Fe作阴极、C作阳极,电解氯化钠溶液得到氢氧化钠、氯气和氢气,电解方程式为:2Cl-+2H2O
| ||
故答案为:Fe-2e-=Fe2+;2Cl-+2H2O
| ||
(5)室温下,Al(OH)3的Ksp或溶解度远大于Fe(OH)3,向浓度均为0.1mol?L?1的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液,NaOH先和Fe(NO3)3反应生成Fe(OH)3,当铁离子完全反应后,Al(NO3)3再和NaOH反应生成Al(OH)3沉淀,但Al元素完全以Al(OH)3形式存在时,如果继续滴加NaOH溶液,Al(OH)3转化为NaAlO2而消失,所以滴加NaOH开始时没有氢氧化铝沉淀生成,当铁离子完全沉淀后再生成氢氧化铝沉淀,最后氢氧化铝完全溶解生成偏铝酸钠,因为硝酸铁和硝酸铝的浓度相等,则开始时不产生沉淀、生成氢氧化铝沉淀、氢氧化铝沉淀完全溶解需要NaOH的体积之比为3:3:1,所以其图象为
 ,故答案为:
,故答案为: .
.
点评:本题考查元素周期表和元素周期律综合应用,侧重考查学生分析问题、解答问题能力,涉及原子结构、元素周期律、物质性质、原电池和电解池原理等知识点,综合性较强,难点是(5)题图象画法,要根据方程式中各个物理量之间的关系式解答,难度中等.

练习册系列答案
相关题目
下列方程式不能正确解释实验事实的是( )
| A、0.l mol?L-l CH3COOH溶液的pH>1:CH3COOH?CH3COO-+H+ |
| B、Na2CO3溶液能使酚酞试液变红:CO32-+H2O?HCO3-+OH- |
| C、铁溶于稀硝酸,溶液变黄:3Fe+8H++2NO3-?3Fe2++2NO↑+4H2O |
| D、向Mg(OH)2悬浊液中加入FeCl3溶液,出现红褐色沉淀:3Mg(OH)2(s)+2Fe3+(aq)?2Fe(OH)3(s)+3Mg2+(aq) |
已知25℃、101kPa下,碳、氢气、乙烯和葡萄糖的燃烧热依次是393.5kJ/mol、285.8kJ/mol、1411.0kJ/mol、2800kJ/mol,则下列热化学方程式正确的是( )
A、C(s)+
| ||
| B、2H2(g)+O2(g)═2H2O(g)△H=+571.6kJ/mol | ||
| C、C2H4(g)+3O2(g)═2CO2(g)+2H2O(g)△H=-1411.0kJ/mol-1 | ||
D、
|
在水溶液中能大量共存的一组离子是( )
| A、Na+、Al3+、Cl-、CO32- |
| B、Cu2+、Fe3+、Cl-、SO42- |
| C、NH4+、Cl-、OH-、HCO3- |
| D、H+、Fe2+、Cl-、NO3- |
 是一种白色晶体,其酸及盐均为强氧化剂.
是一种白色晶体,其酸及盐均为强氧化剂.