题目内容
(9分)(1)在标准状况下,将224 L HCl气体溶于635 mL水中,所得盐酸的密度为
1.18 g·cm-3。试计算:
①所得盐酸物质的量浓度是 。
②取出这种盐酸10 mL,稀释至118 mL,所得稀盐酸的物质的量浓度是 。如取10 mL盐酸时仰视其他操作均正确得稀盐酸浓度 。(填“偏大”、 “等于”、“偏小”)
③在40.0 mL 0.065 mol·L-1 Na2CO3溶液中,逐渐加入(2)所稀释的稀盐酸,边加边振荡。若使反应不产生CO2气体,加入稀盐酸的体积最多不超过 mL。
(2)配制0.80 mol·L-1 NaOH溶液475 mL,回答下列问题:
①根据计算用托盘天平称取NaOH的质量为__________g。在实验中其他操作均正确,若容量瓶用蒸馏水洗涤后未干燥,则所得溶液浓度_______0.80 mol·L-1(填“大于”、“等于”或“小于”,下同)。若还未等溶液冷却就定容了,则所得溶液浓度__________0.80 mol·L-1。
②0.80 mol·L-1 NaOH溶液质量分数 3.2%,和等质量的水混合溶液浓度 0.40 mol·L-1
(1)①11.8mol/L ②1mol/L 偏大 ③2.6
(2)①16.0 等于 大于 ②小于 小于
【解析】
试题分析:(1)①标准状况下,将224 L HCl气体溶于635 mL水中,HCl的物质的是224L/22.4L/mol=10mol,质量是10mol×36.5g/mol=365g,水的质量是635g,所得盐酸的质量是365+635=1000g,所得盐酸的密度为1.18 g·cm-3,所以盐酸的体积是1000g/1.18 g·cm-3=1/1.18L,所以盐酸的物质的量浓度是10mol/1/1.18L=11.8mol/L;②取出10mL,则10mL盐酸的物质的量是0.01L×11.8mol/L=0.118mol,稀释至118 mL,则所得溶液的物质的量浓度是0.118mol/0.118L=1mol/L;如取10 mL盐酸时仰视其他操作均正确,则所取盐酸的体积大于10mL,所以所得溶液的浓度偏大;③若使反应不产生CO2气体,则应生成碳酸氢钠根据Na2CO3~HCl得,HCl的物质的量是0.065 mol·L-1×0.04L=0.0026mol,则需要1mol/L的盐酸的体积是2.6mL;
(2)①配制0.80 mol·L-1 NaOH溶液475 mL,根据容量瓶的规格,应配制500mL的溶液,所需NaOH的物质的量是0.5L×0.80 mol·L-1=0.4mol,则NaOH的质量是0.4mol×40g/mol=16.0g;容量瓶内有蒸馏水对实验结果无影响,所以得到的溶液的物质的量浓度仍是0.80 mol·L-1;未等溶液冷却就定容了,则会造成冷却后溶液的体积减小,实际溶液的体积小于500mL,所配溶液的浓度大于0.80 mol·L-1;
②0.80 mol·L-1NaOH溶液的体积是500mL,其质量大于500mL水的质量500g,若溶液质量是500g,则氢氧化钠的质量分数是16.0g/500g×100%=3.2%,所以实际溶液的质量分数将小于3.2%;等质量的水与0.80 mol·L-1NaOH溶液相比水的体积将大于氢氧化钠溶液的体积,所以0.80 mol·L-1 NaOH溶液和等质量的水混合溶液浓度将小于0.40 mol·L-1。
考点:考查溶液浓度的计算

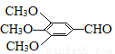 )和抗癫痫药物H(
)和抗癫痫药物H(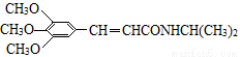 )的路线如下(部分反应略去条件和试剂):
)的路线如下(部分反应略去条件和试剂): 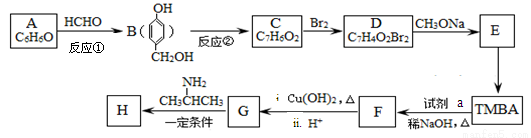
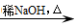
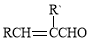 + H2O(R、R’表示烃基或氢)
+ H2O(R、R’表示烃基或氢)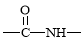 )有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式 。
)有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式 。