题目内容
某有机物A 3.1g在氧气中完全燃烧,将燃烧后的混合物通入过量澄清石灰水中,石灰水增重7.1g(设燃烧产物全部被吸收),经过过滤得到10g沉淀.已知该有机物蒸气是相同条件下氢气密度的31倍.
(1)用化学式回答:10g沉淀物的成份是 ;7.1g质量包含了燃烧生成的CO2和 的总质量.
(2)请计算(写出计算过程):该有机物的分子式,并写出它属于醇类的结构简式.
(1)用化学式回答:10g沉淀物的成份是
(2)请计算(写出计算过程):该有机物的分子式,并写出它属于醇类的结构简式.
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:(1)10g沉淀为碳酸钙的质量,石灰水增重7.1g为燃烧生成的二氧化碳与水的质量;
(2)根据n=
计算碳酸钙的物质的量,再根据碳元素守恒计算n(CO2)、n(C),根据m=nM计算m(CO2),进而计算水的质量,再计算n(H),根据质量守恒定律计算有机物中O原子物质的量,确定有机物的最简式.根据有机物蒸气是相同条件下氢气密度的31倍,计算有机物相对分子质量,结合最简式确定分子式,再书写属于醇类的结构简式.
(2)根据n=
| m |
| M |
解答:
解:(1)10g沉淀为碳酸钙的质量,石灰水增重7.1g为燃烧生成的二氧化碳与水的质量,
故答案为:CaCO3; H2O;
(2)由已知条件得:m(CO2)+m(H2O)=7.1 g,
n(C)=n(CO2)=n(CaCO3)=
=0.1 mol,
故m(CO2)=0.1mol×44g/mol=4.4g,n(H)=2n(H2O)=2×
=0.3 mol
n(O)=
=0.1mol,
所以 n (C):n (H):n(O)=0.1:0.3:0.1=1:3:1.故A物质的实验式为CH3O,
A物质的实验式的式量为:M(CH3O)=31,
机物的摩尔质量=M(H2)×31=2 g/mol×31=62 g/mol
所以A物质的分子式为C2H6O2,
它属于醇的结构简式为HO-CH2-CH2-OH,
答:该有机物的分子式为C2H6O2,属于醇类的结构简式为HO-CH2-CH2-OH.
故答案为:CaCO3; H2O;
(2)由已知条件得:m(CO2)+m(H2O)=7.1 g,
n(C)=n(CO2)=n(CaCO3)=
| 10g |
| 100g/mol |
故m(CO2)=0.1mol×44g/mol=4.4g,n(H)=2n(H2O)=2×
| 7.1g-4.4g |
| 18g/mol |
n(O)=
| 3.1g-0.1mol×12g/mol-0.3mol×1g/mol |
| 16g/mol |
所以 n (C):n (H):n(O)=0.1:0.3:0.1=1:3:1.故A物质的实验式为CH3O,
A物质的实验式的式量为:M(CH3O)=31,
机物的摩尔质量=M(H2)×31=2 g/mol×31=62 g/mol
所以A物质的分子式为C2H6O2,
它属于醇的结构简式为HO-CH2-CH2-OH,
答:该有机物的分子式为C2H6O2,属于醇类的结构简式为HO-CH2-CH2-OH.
点评:本题考查有机物分子式确定、限制条件同分异构体书写等,难度不大,理解燃烧法利用原子守恒确定有机物分子式.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
现有氧化银、氧化镁、氧化铝的混合物,按如图所示的方法制取金属单质,下列叙述正确的是( )


| A、试剂X可能是葡萄糖 |
| B、试剂Z一定是CO2 |
| C、工业上可用CO还原固体2制取金属2 |
| D、工业上用固体3经一步反应制取金属3 |
 某研究性学习小组用电解CuSO4溶液的方法测定铜的相对原子质量(装置如图),实验中测得某电极的质量增重为m g,已知氧元素相对原子质量为16.请回答:
某研究性学习小组用电解CuSO4溶液的方法测定铜的相对原子质量(装置如图),实验中测得某电极的质量增重为m g,已知氧元素相对原子质量为16.请回答:
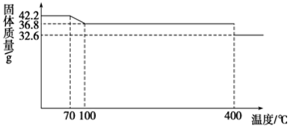 食盐中的抗结剂是亚铁氰化钾,其化学式为K4[Fe(CN)6]?3H2O.42.2g K4[Fe(CN)6]?3H2O样品受热脱水过程的热重曲线(样品质量随温度的变化曲线)如图所示.
食盐中的抗结剂是亚铁氰化钾,其化学式为K4[Fe(CN)6]?3H2O.42.2g K4[Fe(CN)6]?3H2O样品受热脱水过程的热重曲线(样品质量随温度的变化曲线)如图所示.