题目内容
【题目】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是海水综合利用的一个方面。
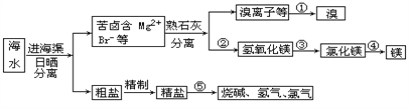
请回答下列问题:
(1)①步主要反应的的离子方程式:_____________________________________________。
(2)分离出氢氧化镁的操作为________________________________,
第③步需要加入________________________________________。
(3)将粗食盐中含有的Mg2+、Ca2+和SO42—等杂质除去,加入的试剂有(按加入顺序填入_________________(只要求填一组合理的答案即可) 。
【答案】 2Br-+Cl2==2Cl-+Br2 过滤 盐酸 氯化钡溶液,氢氧化钠溶液,碳酸钠溶液,盐酸;或氢氧化钠溶液,氯化钡溶液,碳酸钠溶液,盐酸;或氯化钡溶液,碳酸钠溶液,氢氧化钠溶液,盐酸
【解析】(1)向含有溴离子的溶液中加入氯水主要发生:2Br-+Cl2=2Cl-+Br2 ,然后萃取得到Br2;答案为:2Br-+Cl2=2Cl-+Br2 。
(2)分离出氢氧化镁属于分离溶液和固体,分离出氢氧化镁的操作为过滤,将![]() 溶于稀盐酸得到
溶于稀盐酸得到![]() ,答案是:过滤;盐酸;
,答案是:过滤;盐酸;
(3)SO42-、Ca2+、Mg2+等分别与BaCl2溶液、 Na2CO3溶液、NaOH溶液反应生成沉淀,可再通过过滤除去。Na2CO3溶液能除去过量的BaCl2溶液,盐酸能除去过量的 Na2CO3溶液和NaOH溶液,所以应先加BaCl2溶液再加 Na2CO3溶液、氢氧化钠溶液,最后加入盐酸;或加BaCl2溶液、NaOH溶液、碳酸钠溶液、盐酸;(或NaOH溶液、BaCl2溶液、碳酸钠溶液、盐酸)。答案为:氯化钡溶液,氢氧化钠溶液,碳酸钠溶液,盐酸;或氢氧化钠溶液,氯化钡溶液,碳酸钠溶液,盐酸;或氯化钡溶液,碳酸钠溶液,氢氧化钠溶液,盐酸