题目内容
13. 消除大气污染有多种方法.
消除大气污染有多种方法.(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1
②CH4(g)+2NO2(g)═N2 (g)+CO2(g)+2H2O(g)△H=-867kJ•mol-1
③H2O(g)═H2O(l)△H=-44.0kJ•mol-1
写出CH4(g)与NO(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(l)△H=-1248kJ•mol-1.
(2)利用Fe2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理.已知含SO2的废气通入含Fe2+、Fe3+的溶液时,首先是Fe3+被还原成Fe2+,接着Fe2+再被氧化成Fe3+.后一个反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O.
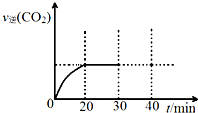
(3)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2(g)+CO2 (g).某研究小组向密闭的真空容器中(假设容器体积不变,固体试样体积忽略不计)加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如表:
| 浓度/mol•L-1 时间/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
②根据表中数据,计算T1℃时该反应的平衡常数K=0.56(保留两位小数).
③一定温度下,随着NO的起始浓度增大,则NO的平衡转化率不变(填“增大”、“不变”或“减小”).
④请在图中画出30min至40min的变化曲线.
分析 (1)利用盖斯定律②×2-①+③×2得到热化学反应方程式;
(2)Fe3+被SO2还原成Fe2+,接着Fe2+再被氧气氧化成Fe3+;
(3)①根据v=$\frac{△c}{△t}$计算v(CO2)
②20min处于平衡状态,根据K=$\frac{c({N}_{2})×c(C{O}_{2})}{{c}^{2}(NO)}$计算平衡常数;
③一定温度下,随着NO的起始浓度增大,等效为增大压强,不影响平衡移动;
④30min~40min之间,NO浓度减小0.08mol/L,N2浓度增大0.04mol/L,CO2浓度减小0.13mol/L,应是减小二氧化碳的浓度,瞬间减小二氧化碳的浓度为(0.3+0.04)mol/L-0.17mol/L=0.17mol/L,平衡时浓度为0.17mol/L.
解答 解:(1)①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1
②CH4(g)+2NO2(g)═N2 (g)+CO2(g)+2H2O(g)△H=-867kJ•mol-1
③H2O(g)═H2O(l)△H=-44.0kJ•mol-1
利用盖斯定律②×2-①+③×2得到热化学反应方程式:CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(l)△H=-1248 kJ•mol-1,
故答案为:CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(l)△H=-1248 kJ•mol-1;
(2)Fe3+被SO2还原成Fe2+,接着Fe2+再被氧气氧化成Fe3+,离子方程式为:4Fe2++O2+4H+═4Fe3++2H2O,
故答案为:4Fe2++O2+4H+═4Fe3++2H2O;
(3)①10min~20min以v(CO2) 表示的反应速率=$\frac{(0.3-0.21)mol•{L}^{-1}}{(20-10)min}$=0.009 mol•L-1•min-1,
故答案为:0.009 mol•L-1•min-1;
②20min处于平衡状态,平衡常数K=$\frac{c({N}_{2})×c(C{O}_{2})}{{c}^{2}(NO)}$=$\frac{0.3×0.3}{0.{4}^{2}}$=0.56,
故答案为:0.56;
③一定温度下,随着NO的起始浓度增大,等效为增大压强,不影响平衡移动,则NO的平衡转化率不变,
故答案为:不变;
④30min~40min之间,NO浓度减小0.08mol/L,N2浓度增大0.04mol/L,CO2浓度减小0.13mol/L,应是减小二氧化碳的浓度,瞬间减小二氧化碳的浓度为(0.3+0.04)mol/L-0.17mol/L=0.17mol/L,该瞬间二氧化碳浓度为0.13mol/L,平衡时浓度为0.17mol/L,则30min至40minCO2浓度的变化曲线图象为: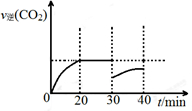 ,
,
故答案为: .
.
点评 本题考查化学平衡计算与影响因素、平衡状态判断、平衡常数、反应速率、热化学方程式书写等,(3)中作图为易错点,注意二氧化碳的瞬间浓度与平衡浓度.

| A. |  CuSO4溶液 | B. |  ZnSO4溶液 | ||
| C. |  酒精 | D. | 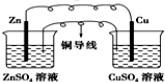 |
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
(1)上述实验中发生反应的化学方程式有Zn+CuSO4=ZnSO4+Cu,Zn+H2SO4=ZnSO4+H2↑;
(2)硫酸铜溶液可以加快氢气生成速率的原因是CuSO4 与Zn反应产生的 Cu 与Zn形成铜锌原电池,加快了氢气产生的速率;
(3)实验室中现有Na2SO4、MgSO4、AgNO3、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是AgNO3;
(4)要加快上述实验中气体产生的速率,还可采取的措施有升高反应温度;适当增加硫酸的浓度、增加锌粒的表面积等 (任答一种);
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列的实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL | 30 | V1 | 30 | 30 | 30 | 30 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | 20 | V8 | V9 | V10 | 10 | 0 |
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因当加入一定量的硫酸铜后,生成的单质铜会沉积在锌的表面,降低了锌与溶液的接触面积.
(1)常温下,用CO、O2和水在三苯基膦钯的催化下即可制得H2O2.相对于电解氢氧化钠溶液制H2O2,该方法具有的优点是安全、能耗低.
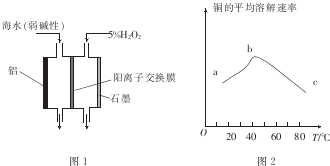
(2)图1是铝/过氧化氢电池结构示意图.铝电极为负极(填“正极”或“负极”),石墨电极的电极反应式为H2O2+2e-=2OH-
(3)印刷电路板中的金属铜可用10%的H2O2溶液和3.0mol.L-l的H2S04溶液处理,其他条件相同时,测得铜的平均溶解速率与温度的关系如图2所示.其中bc段曲线变化的主要原因是随着温度的升高,双氧水的分解速率加快
(4)为研究硫酸铁的量对过氧化氢分解速率的影响,某同学设计了如下一系列的实验.将表中所给的溶液分别加入A、B、C、D 4个反应瓶中,收集产生的气体,记录数据.
| 实验 体积/mL 液体 | A | B | C | D |
| 0.4mol.L-1Fe2(SO4)3溶液 | 0 | 1.8 | 2.0 | V1 |
| 30%H2O2溶液 | 20.0 | 20.0 | 20.0 | 20.0 |
| HO2 | V2 | V3 | 15.0 | 13.8 |
②上表中V3=15.2.
| A. | 卤素是典型的非金属元素,因此不能与其他非金属元素化合 | |
| B. | 卤素单质越活泼,其熔、沸点就越高 | |
| C. | 卤素单质都能和水剧烈反应 | |
| D. | 卤素单质都能和H2反应,且气态氢化物的稳定性随单质氧化性的增强而增强 |
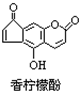
| A. | 它的分子式为C13H9O4 | |
| B. | 它与H2发生加成反应,1mol最多可消耗7mol H2 | |
| C. | 它与溴水发生反应,1mol最多消耗3mol Br2 | |
| D. | 它与NaOH溶液反应,1mol最多消耗2molNaOH |
①Ba(OH)2溶液②CaCl2溶液 ③H2S溶液 ④Ba(NO3)2溶液 ⑤Na2SiO3溶液.
| A. | ③④⑤ | B. | ②③⑤ | C. | ①③④⑤ | D. | ②③④⑤ |
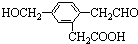 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )①加成 ②水解 ③取代 ④氧化 ⑤还原 ⑥消去.
| A. | ②③④ | B. | ①③⑤⑥ | C. | ①③④⑤ | D. | ①③④⑤⑥ |