题目内容
在H2SO4、Fe2(SO4)3和CuSO4的混合溶液中,投入一定量的铁屑,充分反应后,发现铁屑有剩余,溶液中存在的阳离子有( )
| A、只有Fe2+ |
| B、有Fe2+和Fe3+ |
| C、有Cu2+和Fe2+ |
| D、有H+和Fe3+ |
考点:氧化还原反应,离子反应发生的条件,铁盐和亚铁盐的相互转变
专题:离子反应专题
分析:氧化性为Fe3+>Cu2+>H+,则投入一定量的铁屑,充分反应后,发现铁屑有剩余,三种离子均完全反应,以此来解答.
解答:
解:氧化性为Fe3+>Cu2+>H+,则投入一定量的铁屑,充分反应后,发现铁屑有剩余,三种离子均完全反应,且反应均生成Fe2+,
故选A.
故选A.
点评:本题考查氧化还原反应,为高频考点,把握氧化性的强弱及发生的反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
常温下,下列物质中能与SiO2发生反应的是( )
| A、硫酸 | B、氢氟酸 | C、水 | D、稀盐酸 |
用NA表示阿伏德罗常数的值,下列叙述正确的是( )
| A、标准状况下,22.4LH2O含有的分子数为1 NA |
| B、常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA |
| C、通常状况下,60 g SiO2晶体中含有SiO2分子数为1 NA |
| D、物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为1 NA |
设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、78g Na2O2与足量水充分反应时电子转移数为2NA |
| B、1 mol Na完全转化为Na2O2时,失去的电子数目为2NA |
| C、4℃、101.3kPa时,54mL H2O中含有的分子数为3NA |
| D、2L1mol/L Na2SO4溶液中离子总数为3NA |
下列化学用语错误的是( )
A、Na+的结构示意图: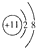 |
B、水分子的电子式: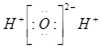 |
| C、二氧化碳的结构式:O=C=O |
| D、硫酸钠的电离方程式:Na2SO4=2Na++SO42- |
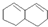 在较高温度下和Br2按物质的量之比1:1发生加成反应的方程
在较高温度下和Br2按物质的量之比1:1发生加成反应的方程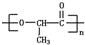 是由一种单体缩聚而成的,该单体的结构简式为
是由一种单体缩聚而成的,该单体的结构简式为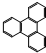 的一氯取代物有
的一氯取代物有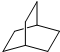 的二氯取代物有
的二氯取代物有 实验室中有一未知浓度的稀盐酸,某学生在实验室中进行测定盐酸浓度的实验,请完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生在实验室中进行测定盐酸浓度的实验,请完成下列填空: