题目内容
将物质的量相等的H2和I2气充入密闭容器,进行反应H2(g)+I2(g)?2HI(g),测得2min时v(HI)为0.1mol?(L?min)-1,I2(g)的浓度为0.4mol?L-1,试确定:
(1)H2和I2的反应速率为 .
(2)H2和I2的起始浓度为 .
(3)2min 末HI的浓度为 .
(1)H2和I2的反应速率为
(2)H2和I2的起始浓度为
(3)2min 末HI的浓度为
考点:化学平衡的计算
专题:化学平衡专题
分析:(1)同一可逆反应中同一时间段内,各物质的反应速率之比等于其计量数之比,从而计算氢气、碘的反应速率;
(2)根据△c=vt计算参加反应的碘的物质的量浓度,H2和I2的起始浓度=2min末碘蒸气浓度+参加反应的碘蒸气浓度;
(3)HI为生成物,根据△c=vt计算出2min末HI的浓度.
(2)根据△c=vt计算参加反应的碘的物质的量浓度,H2和I2的起始浓度=2min末碘蒸气浓度+参加反应的碘蒸气浓度;
(3)HI为生成物,根据△c=vt计算出2min末HI的浓度.
解答:
解:(1)同一可逆反应中同一时间段内,各物质的反应速率之比等于其计量数之比,所以H2和I2的反应速率为v(H2)=v(I2)=
v(HI)=
×0.1mol?(L?min)-1=0.05mol?(L?min)-1,
故答案为:0.05mol?(L?min)-1;
(2)参加反应的碘蒸气浓度:△c(I2)=vt=0.05mol/(L.min)×2min=0.1mol/L,碘蒸气的起始浓度为:c(I2)=0.1mol/L+0.4mol/L=0.5mol/L;
氢气和碘单质的物质的量相等,则起始浓度:c(H2)=c(I2)=0.5mol/L,
故答案为:0.5mol/L;
(3)HI为生成物,测得2min时v(HI)=0.1mol?(L?min)-1,则2min时生成HI的物质的量浓度为:c(HI)=0.1mol?(L?min)-1×2min=0.2 mol?L-1,
故答案为:0.2mol?L-1.
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:0.05mol?(L?min)-1;
(2)参加反应的碘蒸气浓度:△c(I2)=vt=0.05mol/(L.min)×2min=0.1mol/L,碘蒸气的起始浓度为:c(I2)=0.1mol/L+0.4mol/L=0.5mol/L;
氢气和碘单质的物质的量相等,则起始浓度:c(H2)=c(I2)=0.5mol/L,
故答案为:0.5mol/L;
(3)HI为生成物,测得2min时v(HI)=0.1mol?(L?min)-1,则2min时生成HI的物质的量浓度为:c(HI)=0.1mol?(L?min)-1×2min=0.2 mol?L-1,
故答案为:0.2mol?L-1.
点评:本题考查了化学平衡、化学反应速率的计算,题目难度中等,注意掌握化学反应速率与化学计量数的关系,明确化学反应速率的概念及计算方法,试题侧重考查了学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
在紫外线的作用下,氧气可生成臭氧:3O2
2O3,一定条件下的恒容容器中,该反应达到平衡状态的标志是( )
| 紫外线 |
| A、单位时间内生成2 mol O3,同时消耗3 mol O2 |
| B、O2的消耗速率0.3 mol?L-1?s-1,O3的消耗速率0.2 mol?L-1?s-1 |
| C、容器内,2种气体O3、O2浓度相等 |
| D、气体的密度不在改变. |
下列说法中,正确的是( )
| A、两种难溶盐电解质,其中Ksp小的溶解度一定小 |
| B、溶液中存在两种可以与同一沉淀剂生成沉淀的离子,则Ksp小的一定先沉淀 |
| C、Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关 |
| D、凡是能自发进行的化学反应,一定是△H<0、△S>0 |
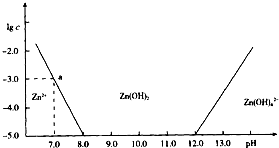 已知Zn2+与碱反应可生成白色沉淀,碱过量,白色沉淀溶解生成Zn(OH)42-.如图是向含Zn2+的溶液中逐滴加入氢氧化钠溶液的变化过程示意图,横坐标为溶液的pH,纵坐标为Zn2+离子或Zn(OH)42-离子物质的量浓度的对数值.回答下列问题.
已知Zn2+与碱反应可生成白色沉淀,碱过量,白色沉淀溶解生成Zn(OH)42-.如图是向含Zn2+的溶液中逐滴加入氢氧化钠溶液的变化过程示意图,横坐标为溶液的pH,纵坐标为Zn2+离子或Zn(OH)42-离子物质的量浓度的对数值.回答下列问题.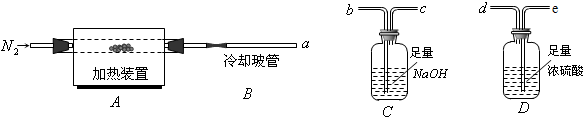
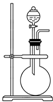 如图是实验室制取某些气体的装置.
如图是实验室制取某些气体的装置.