题目内容
某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X.
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是 .
(2)已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为 .
(3)根据上述反应可推知 .
A.氧化性:KBrO3>H3AsO4 B.氧化性:H3AsO4>KBrO3
C.还原性:AsH3>X D.还原性:X>AsH3.
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是
(2)已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为
(3)根据上述反应可推知
A.氧化性:KBrO3>H3AsO4 B.氧化性:H3AsO4>KBrO3
C.还原性:AsH3>X D.还原性:X>AsH3.
考点:氧化还原反应
专题:氧化还原反应专题
分析:由信息可知,该反应中氧化剂是KBrO3,还原剂是AsH3,溴元素化合价变化为由+5价降低,As元素化合价变化为-3→+5价,
(1)KBrO3在反应中得到电子,被还原,而还原剂被氧化;
(2)根据溴元素化合价的降低情况来计算;
(3)氧化剂的氧化性最强,还原剂的还原性最强,氧化剂对应的产物叫还原产物.
(1)KBrO3在反应中得到电子,被还原,而还原剂被氧化;
(2)根据溴元素化合价的降低情况来计算;
(3)氧化剂的氧化性最强,还原剂的还原性最强,氧化剂对应的产物叫还原产物.
解答:
解:(1)KBrO3在反应中得到电子,所以KBrO3是氧化剂,AsH3变成了H3AsO4,砷元素化合价升高,所以还原剂是AsH3,故答案为:AsH3;
(2)设X中溴元素的化合价为x,则0.2mol(5-x)=1mol,所以x=0,故X为Br2,故答案为:Br2;
(3)在反应中,氧化剂为KBrO3,还原剂为AsH3,氧化产物为H3AsO4,还原产物为Br2,
由氧化剂的氧化性大于氧化产物的氧化性可知KBrO3>H3AsO4,由还原剂的还原性大于还原产物的还原性可知AsH3>X (Br2),
故答案为:AC.
(2)设X中溴元素的化合价为x,则0.2mol(5-x)=1mol,所以x=0,故X为Br2,故答案为:Br2;
(3)在反应中,氧化剂为KBrO3,还原剂为AsH3,氧化产物为H3AsO4,还原产物为Br2,
由氧化剂的氧化性大于氧化产物的氧化性可知KBrO3>H3AsO4,由还原剂的还原性大于还原产物的还原性可知AsH3>X (Br2),
故答案为:AC.
点评:本题考查氧化还原反应,为高考常见题型,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念和转移电子的考查,题目难度不大.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
下列表示电子转移的方法正确的是( )
A、 |
B、 |
C、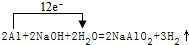 |
D、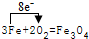 |
下列各溶液中,Na+浓度最大的是( )
| A、0.5 L 9.5mol/L的NaOH溶液 |
| B、2 L 0.4mol/L的NaN03溶液 |
| C、3L 0.3moI/L的NaCl溶液 |
| D、1 L 0.2mol/L的Na3P04溶液 |
由无水醋酸钠与碱石灰共热可得到甲烷.你预测将无水苯乙酸钠与碱石灰共热时,所得的有机物主要是( )
| A、苯 | B、甲苯 |
| C、乙苯 | D、苯甲酸钠与甲烷 |
 现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.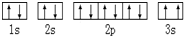 ,违背了
,违背了