题目内容
1.除去乙烷中的乙烯,最好用( )| A. | 通过溴水 | B. | 通过溴的四氯化碳溶液 | ||
| C. | 通过酸性KMnO4溶液 | D. | 在催化剂加热时通入氢气 |
分析 乙烯与溴水发生加成反应,乙烷不能,溴的四氯化碳溶液中溴的浓度大,吸收效果好,以此来解答.
解答 解:A.乙烯与溴水反应,而乙烷不能,可除杂,但溴水中溴的含量较低,不是最好方法,故A不选;
B.乙烯与溴发生加成反应,乙烷不能,溴的四氯化碳溶液中溴的浓度大,吸收效果好,故B选;
C.乙烯被氧化生成二氧化碳,引入新杂质,故C不选;
D.易引入新杂质氢气,故D不选;
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异、混合物分离原理为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
13.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 0.2 mol铁粉与足量水蒸气反应生成的H2分子数为0.3NA | |
| B. | 25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | 常温常压下,17g甲基(-14CH3)所含的电子数为9NA | |
| D. | 在1 L 0.1 mol/L的碳酸钠溶液中,氧原子总数为0.3NA |
16.常温下,下列各组离子在特定的溶液中一定能大量共存的是( )
| A. | 0.1 mol•L-1的NaOH溶液:K+、Na+、SO42-、CO32- | |
| B. | 0.1 mol•L-1的Na2CO3溶液:K+、Ba2+、NO3-、Cl- | |
| C. | 0.1 mol•L-1FeCl3溶液:K+、NH4+、I-、SCN- | |
| D. | 使石蕊试液变红的溶液:Ca2+、Na+、ClO-、NO3- |
6.若不考虑立体异构,则分子式为C4H8O2且为酯的同分异构体共( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
13.下列操作中不正确的是( )
| A. | 过滤时玻璃棒与三层滤纸处接触 | |
| B. | 酒精和水的混合物可以通过蒸馏将二者分离开来 | |
| C. | 向试管中滴加液体时,胶头滴管应紧贴试管内壁 | |
| D. | KNO3中混有少量的NaCl,可通过重结晶实验将杂质出去 |
10.已知2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ/mol
根据以上热化学方程式,下列判断正确的是( )
Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ/mol
根据以上热化学方程式,下列判断正确的是( )
| A. | CO的燃烧热为283 Kj | |
| B. | 2 mol CO2(g)与2 mol Na2O2(s)反应放出452 kJ热量时,电子转移数约为1.204×1024 | |
| C. | 2Na2O2(s)+2CO2(s)═2Na2CO3(s)+O2(g)△H<-452 kJ/mol | |
| D. | 如图可表示CO生成CO2,的反应过程和能量关系 |
11.下列实验“操作和现象”与“结论”对应关系正确的是( )
| 操作和现象 | 结论 | |
| A | 向FeCl3和CuCl2混合溶液中加入铁粉,有红色固体析出 | 氧化性:Cu2+>Fe3+ |
| B | 用石墨作电极电解MgSO4溶液,某电极附近有白色沉淀生成 | 该电极为阳极 |
| C | 处理锅炉水垢中的CaSO4时,依次加入饱和Na2CO3溶液和盐酸,水垢溶解 | 溶度积:Ksp(CaCO3)<Ksp(CaSO4) |
| D | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有Ag+ |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |

 ②
② ③
③ ④
④
 +4Br2→
+4Br2→ +3HBr.
+3HBr. $\stackrel{试剂1}{→}$
$\stackrel{试剂1}{→}$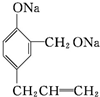 $\stackrel{试剂2}{→}$
$\stackrel{试剂2}{→}$ ,则试剂1为Na,试剂2为稀硫酸(或其他合理答案).
,则试剂1为Na,试剂2为稀硫酸(或其他合理答案).