题目内容
11.有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数,B元素可分别与A、C、D、E生成RB2型化合物,并知在DB2和EB2中,D与B的质量比为7:8,E与B的质量比为1:1.根据以上条件,回答下列问题:(1)写出D元素符号Si.
(2)写出D原子的价电子排布式3s23p2.
(3)写出A元素在B中完全燃烧的化学方程式C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2.
(4)指出E元素在元素周期表中的位置第三周期ⅥA族.
(5)比较A、B、C三种元素的第一电离能的大小顺序N>O>C(用元素符号表示).
(6)比较元素D和E的电负性的相对大小Si<S(用元素符号表示).
分析 有A、B、C、D、E五种元素,A原子最外层p能级的电子数等于次外层的电子总数,p能级电子数不超过6,故原子只能有2个电子层,核外电子排布为1s22s22p2,故A为碳元素;A、B、C属于同一周期,B元素可分别与A、C、D、E生成RB2型化合物,B应为O元素,C为N元素;在DB2和EB2中,D与B的质量比为7:8,则有Mr(D):Mr(O)=7:4,故M(D)=7×$\frac{16}{4}$=28,D应为Si元素;E与B的质量比为1:1,则Mr(E)=2M(O)=2×16=32,所以E为S元素,据此解答.
解答 解:有A、B、C、D、E五种元素,A原子最外层p能级的电子数等于次外层的电子总数,p能级电子数不超过6,故原子只能有2个电子层,核外电子排布为1s22s22p2,故A为碳元素;A、B、C属于同一周期,B元素可分别与A、C、D、E生成RB2型化合物,B应为O元素,C为N元素;在DB2和EB2中,D与B的质量比为7:8,则有Mr(D):Mr(O)=7:4,故M(D)=7×$\frac{16}{4}$=28,D应为Si元素;E与B的质量比为1:1,则Mr(E)=2M(O)=2×16=32,所以E为S元素.
(1)由上述分析可知,D为Si元素,故答案为:Si;
(2)D为Si元素,价电子排布式为3s23p2,故答案为:3s23p2;
(3)碳在氧气中完全燃烧生成二氧化碳,反应方程式为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,故答案为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;
(4)E为S元素,处于周期表中第三周期ⅥA族,故答案为:第三周期ⅥA族;
(5)同周期随原子序数增大,第一电离能呈增大趋势,由于N原子2p轨道为半充满状态,能量较低,第一电离能高于同周期相邻元素,所以第一电离能N>O>C,故答案为:N>O>C;
(6)Si、S同周期,随原子序数增大,电负性增大,故电负性Si<S,故答案为:Si<S.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,注意理解掌握同周期元素第一电离能异常情况.

 名校课堂系列答案
名校课堂系列答案(1)实验室以绿矾为原料,通过以下过程制备磁性Fe3O4胶体粒子:
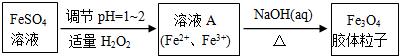
①写出FeSO4溶液转化为溶液A发生反应的离子方程式:2Fe2++H2O2+2H+═2Fe3++2H2O.
②Fe3O4胶体粒子不能用过滤法实现分离,理由是胶体粒子的直径较小(在10-7~10-9m),过滤时可透过滤纸.
③一定条件下,Fe3+水解生成聚合物的离子方程式为:xFe3++yH2O?Fex(OH)y(3x-y)++yH+
欲使平衡正向移动可采用的方法有abd(填字母).
a.加水稀释 b.加入少量NaCl溶液
c.降温 d.加入少量Na2CO3固体
④设计一个实验,证明溶液A中既含有Fe3+又含有Fe2+:取少量溶液A于洁净的试管中,加入硫氰化钾溶液,溶液显红色,说明溶液中含有Fe3+;另取少量溶液A于另一洁净的试管中,滴入酸性高锰酸钾溶液,振荡后溶液颜色从紫红色变成黄色说明溶液含有Fe2+.
(2)柠檬酸亚铁(FeC6H6O7)是一种易吸收的高效铁制剂,可由绿矾通过下列反应制备:
FeSO4+Na2CO3═FeCO3↓+Na2SO4 FeCO3+C6H8O7═FeC6H6O7+CO2↑+H2O
下表列出了Fe2+生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe2+ | 5.8 | 8.8 |
②将制得的FeCO3加入到足量柠檬酸溶液中,再加入少量铁粉,80℃下搅拌充分反应.反应结束后,无需过滤,再加入适量的柠檬酸溶液即可除去过量铁粉.该反应的化学方程式为Fe+C6H8O7=FeC6H6O7+H2↑.
③上述溶液经浓缩后,加入适量无水乙醇,静置、过滤、洗涤、干燥,得到柠檬酸亚铁晶体.分离过程中加入无水乙醇的目的是降低柠檬酸亚铁在水中的溶解量,有利于晶体析出.
(3)正常人每天应补充13.0mg左右的铁,如果全部通过服用含FeSO4•7H2O的片剂来补充铁,则正常人每天需服用含64.5mg FeSO4•7H2O的片剂(保留一位小数).
 TiO2在光照射下可使水电解:2H2O$\frac{\underline{\;TiO_{2}\;}}{光}$在2H2↑+O2↑,该过程类似植物的光合作用.如图是光照射下TiO2分解水的装置示意图.下列叙述正确的是( )
TiO2在光照射下可使水电解:2H2O$\frac{\underline{\;TiO_{2}\;}}{光}$在2H2↑+O2↑,该过程类似植物的光合作用.如图是光照射下TiO2分解水的装置示意图.下列叙述正确的是( )| A. | 该装置可以将光能转化为电能,同时也能转化为化学能 | |
| B. | 铂电极上发生的反应为:H2-2e-=2H+ | |
| C. | 该装置工作时,电流由TiO2电极经R流向铂电极 | |
| D. | 该装置工作时,TiO2电极附近溶液的pH变大 |
| A. | Na Mg Al | B. | Na O F | C. | P Si Al | D. | C Si P |
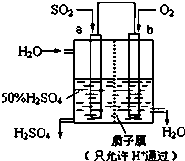
| A. | a为负极,b为正极 | |
| B. | b电极发生氧化反应 | |
| C. | H+从a极向b极移动 | |
| D. | 负极反应式为:SO2+2H2O-2e-=SO42-+4H+ |
| A. | ${\;}_{83}^{209}$Bi比${\;}_{83}^{210}$Bi的质量数小1 | |
| B. | ${\;}_{83}^{209}$Bi和${\;}_{83}^{210}$Bi都含有83个中子 | |
| C. | ${\;}_{83}^{209}$Bi和${\;}_{83}^{210}$Bi的核外电子数不同 | |
| D. | ${\;}_{83}^{209}$Bi和${\;}_{83}^{210}$Bi分别含有126和127个质子 |
| A. | 随着核电荷数增加,碱金属单质的密度逐渐增大 | |
| B. | 随着核电荷数增加,卤素单质的熔沸点逐渐降低 | |
| C. | 随着核电荷数的增加,碱金属单质与水反应的剧烈程度增大 | |
| D. | 随着核电荷数增加,碱金属离子的氧化性逐渐增强,卤素离子的还原性逐渐减弱 |
| A. | 碳碳双键不可旋转所以烯烃一定有顺反异构 | |
| B. | 邻二甲苯只有一种结构可以证明苯分子中无单双健的交替结构 | |
| C. | CH2Cl2无同分异构体可以证明CH4是正四面体的结构 | |
| D. | 乙烯、乙炔是平面型分子,可知CH3-CH=C(CH3)-C≡C-CH3分子中所有的碳原子共面 |
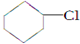 (一氯环己烷)$→_{△②}^{NaOH、乙醇}$
(一氯环己烷)$→_{△②}^{NaOH、乙醇}$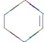 $→_{③}^{Br_{2}的CCl_{4}溶液}$B $\stackrel{④}{→}$
$→_{③}^{Br_{2}的CCl_{4}溶液}$B $\stackrel{④}{→}$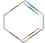
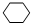 ,名称是环己烷.
,名称是环己烷.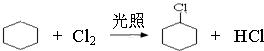 、
、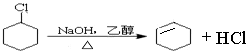 .
.