题目内容
氮氧化物与悬浮在大气中海盐粒子的相互反应:
4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+ Cl2(g),ΔH
2NaNO3(s)+2NO(g)+ Cl2(g),ΔH
在恒温条件下,向2 L恒容密闭容器中加入0.4mol NO2和0.2 mol NaCl,10 min反应达到平衡时n(NaNO3)=0.1mol,NO2的转化率为α。下列叙述中正确的是
A.10min内NO浓度变化表示的速率v(NO)=0.01 mol·L-1·min-1
B.若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率大于α
C.若升高温度,平衡逆向移动,则该反应的ΔH>0
D.若起始时向容器中充入NO2(g) 0.1 mol、NO(g)0.2 mol和Cl2(g)0.1 mol(固体物质足量),则反应将向逆反应方向进行
BD
【解析】
试题分析:A、10 min反应达到平衡时n(NaNO3)=0.1mol,则生成NO的物质的量是0.1mol,浓度是0.1mol÷2L=0.05mol/L,则10min内NO浓度变化表示的速率v(NO)=0.05mol/L÷10min=0.005 mol·L-1·min-1,A错误;B、正方应是体积减小的可逆反应,在反应过程中压强减小,因此若保持其他条件不变,在恒压下进行该反应,有利于平衡向正反应方向减小,则平衡时NO2的转化率大于α,B正确;C、若升高温度,平衡向吸热反应方向进行,因此如果平衡逆向移动,则正方应是放热反应,所以该反应的ΔH<0,C错误;D、根据以上分析可知平衡时NO2(g)、NO(g)和Cl2(g)的浓度分别是0.1mol/L、0.05mol/L、0.025mol/L,所以该温度下平衡常数K=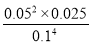 =0.625.则若起始时向容器中充入NO2(g) 0.1 mol、NO(g)0.2 mol和Cl2(g)0.1 mol(固体物质足量),其浓度分别是0.05mol/L、0.1mol/L、0.05mol/L,则此时的浓度熵=
=0.625.则若起始时向容器中充入NO2(g) 0.1 mol、NO(g)0.2 mol和Cl2(g)0.1 mol(固体物质足量),其浓度分别是0.05mol/L、0.1mol/L、0.05mol/L,则此时的浓度熵=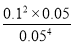 =80>0.625,平衡反应将向逆反应方向进行,D正确,答案选BD。
=80>0.625,平衡反应将向逆反应方向进行,D正确,答案选BD。
考点:考查可逆反应的有关计算

 阅读快车系列答案
阅读快车系列答案(14分)H2O2是一种常用绿色氧化剂,在化学研究中应用广泛。
(1)空气阴极法电解制备H2O2的装置如下图所示,主要原理是在碱性电解质溶液中,通过利用空气中氧气在阴极还原得到H2O2和稀碱的混合物。
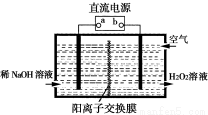
试回答:
①直流电源的a极名称是 。
②阴极电极反应式为 。
③1979年,科学家们用CO、O2和水在三苯膦钯的催化下制得了H2O2。相对于电解法,该方法具有的优点是安全、 。
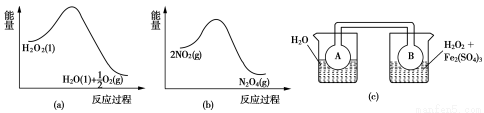
(2)Fe3+对H2O2的分解具有催化作用。利用图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的 (填“深”或“浅”),其原因是 。
(3)用H2O2 和H2SO4 的混合溶液可溶解印刷电路板金属粉末中的铜。反应的离子方程式是 ,控制其它条件相同,印刷电路板的金属粉末用10%H2O2 和3.0mol·L-1H2SO4溶液处理,测得不同温度下铜的平均溶解速率(见下表)
温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
Cu的平均溶解速率 (×10-3mol·min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
当温度高于40℃时,铜的平均溶解速率随着反应温度的升高而下降,其主要原因是 。
 N放出942KJ,
N放出942KJ,
 A.乙烯的结构简式:CH2=CH2 B.二氧化硫分子比例模型:
A.乙烯的结构简式:CH2=CH2 B.二氧化硫分子比例模型: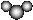
 CuSO4(s) +5H2O(l),热效应为ΔH3。则下列判断正确的是
CuSO4(s) +5H2O(l),热效应为ΔH3。则下列判断正确的是 2H++Cl-+ClO-
2H++Cl-+ClO-