题目内容
如图表示治理汽车尾气所涉及反应的微观过程.下列说法不正确的是( )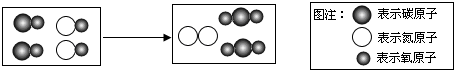

| A、图中单质的化学式为N2 |
| B、该反应使有毒气体转化为无毒气体 |
| C、反应物都属于氧化物 |
| D、反应中原子、分子个数都不变 |
考点:常见的生活环境的污染及治理,"三废"处理与环境保护
专题:
分析:由反应的微观过程图可知,治理汽车尾气所涉及反应为2个CO和2个NO发生反应生成2个二氧化碳和1个氮气,方程式为2CO+2NO═2CO2+N2,据此分析;
解答:
解:由反应的微观过程图可知,方程式为2CO+2NO═2CO2+N2,
A、根据方程式得出单质的化学式为N2,故A正确;
B、根据方程式得出反应前CO和NO是有毒气体,反应后CO2和N2为无毒气体,所以该反应使有毒气体转化为无毒气体,故B正确;
C、根据方程式得出反应物是CO和NO,都属于氧化物,故C正确;
D、根据方程式和质量守恒,反应前后原子个数不变,而分子由4变成3,故D错误;
故选:D;
A、根据方程式得出单质的化学式为N2,故A正确;
B、根据方程式得出反应前CO和NO是有毒气体,反应后CO2和N2为无毒气体,所以该反应使有毒气体转化为无毒气体,故B正确;
C、根据方程式得出反应物是CO和NO,都属于氧化物,故C正确;
D、根据方程式和质量守恒,反应前后原子个数不变,而分子由4变成3,故D错误;
故选:D;
点评:本题主要考查了利用微观过程图分析反应的原理、本质,难度不大,关键要先能由反应的微观过程图写出方程式;

练习册系列答案
相关题目
下列物质在足量氧气中燃烧,能生成黑色固体的是( )
| A、铁丝 | B、红磷 | C、酒精 | D、木炭 |
下列说法正确的是( )
| A、反应A(g)?2B(g);△H,若正反应的活化能为Ea kJ mol-1,逆反应的活化能为Eb kJ?mol-1,则△H=(Ea-Eb)kJ?mol-1 | ||
| B、标准状态下,将0.1 mol?L-1 的氨水溶液中加入少量氯化铵晶体,若混合溶液pH=7,则c(NH4+)=c(Cl-) | ||
| C、足量的锌铜合金与100mL pH=1 稀硫酸反应,反应3s 时测得pH=2,假设反应前后溶液的体积保持不变,则3s 内产生氢气的平均速率是33.6 mL?s-1 | ||
D、将浓度为0.1mol?L-1HF 溶液加水不断稀释过程中,电离度(α)和Ka(HF)保持不变,
|
下表是3种物质的溶解度(20℃),下列说法中正确的是( )
| 物质 | MgCl2 | Mg(OH)2 | MgCO3 |
| 溶解度(g/100g) | 74 | 0.000 84 | 0.01 |
| A、已知MgCO3的Ksp=6.82×10-6 mol2?L-2,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)?c(CO32-)=6.82×10-6 mol2?L-2 |
| B、除去粗盐中含有的MgCl2杂质,最佳除杂试剂为Na2CO3溶液 |
| C、将表中三种物质与水混合,加热、灼烧,最终的固体产物相同 |
| D、用石灰水处理含有Mg2+和HCO3-的硬水,发生的离子反应方程式为Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+MgCO3↓+2H2O |
短周期元素X、Y、Z在元素周期表中的位置如图,关于X、Y、Z的说法正确的是( )


| A、相同条件下,三种元素的单质跟氢气反应时,X单质最剧烈 |
| B、Y的气态氢化物稳定性比Z的气态氢化物的稳定性强 |
| C、ZO2能与Z的最高价氧化物对应的水化物反应生成Z单质 |
| D、由氢、氧和Z元素形成的常见化合物中既含有离子键又含有共价键 |
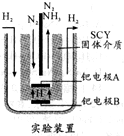 氨是一种重要的化工原料,氨的合成和应用是当前的重要研究内容之一.
氨是一种重要的化工原料,氨的合成和应用是当前的重要研究内容之一.