题目内容
某温度下纯水中C(H+ )=2×10-7 mol/L,若温度不变,滴入稀盐酸使C(H+ )=5×10-6 mol/L,则此时溶液中的C(OH- )= mol/L.
考点:离子积常数
专题:电离平衡与溶液的pH专题
分析:依据纯水存在电离平衡,电离出的氢离子浓度和氢氧根离子浓度相同;在酸溶液、碱溶液、盐溶液中存在离子积常数,Kw随温度变化;依据离子积计算离子浓度.
解答:
解:某温度下纯水中的C(H+)=2×10-7mol/L,则此时溶液中的C(OH-)=2×10-7mol/L;若温度不变,滴入稀盐酸,使C(H+)=5×10-6mol/L,溶液中则溶液中Kw=C(H+)×C(OH-)=4×10-14;
C(OH-)=
=8×10-9mol/L,
故答案为:8×10-9.
C(OH-)=
| 4×10-14 |
| 5×10-6 |
故答案为:8×10-9.
点评:本题考查了水的离子积概念,溶液中离子积的计算判断,注意离子积常数的应用条件和酸溶液中的计算分析应用,题目较简单.

练习册系列答案
相关题目
常温下,将pH=3的盐酸和pH=11的氨水等体积混合,完全反应后,溶液中离子浓度关系正确的是( )
| A、c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| B、c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| C、c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D、c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
足量的铝粉分别和等体积pH=12的NaOH溶液以及pH=2的某酸溶液反应,放出氢气的体积分别为V1、V2,则在相同状况下,V1、V2的关系可能是( )
| A、V1<V2 |
| B、V1=V2 |
| C、V1>V2 |
| D、以上三种情况都有可能 |
在铜-锌-硫酸构成的原电池中,经过一段时间的工作后,下列说法正确的是( )
| A、锌片是负极,铜片上有气泡冒出 |
| B、电流方向是从锌片流向铜片 |
| C、溶液中硫酸的物质的量不变 |
| D、电解液的pH保持不变 |
下列说法正确的是( )
| A、3p3表示3p能级有三个轨道 |
| B、同一原子中,2p、3p、4p能级的轨道数依次增多 |
| C、冰和固体碘晶体中的相互作用力不相同 |
D、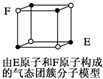 某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE 某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE |
1953年日本水俣湾发生了一起重大的中毒事件,造成人畜大量死亡.科学家分析发现,水俣湾鱼体内甲基汞的含量比周围水体内的甲基汞含量高3000倍,那么甲基汞进入鱼体内的主要方式是 ( )
| A、主动运输 |
| B、渗透作用 |
| C、鳃部交换气体随血液循环 |
| D、水中食物链 |