题目内容
在一定温度下,将CO和水蒸气分别为1 mol、3 mol,在密闭容器中反应:CO+H2O(g)A.1.2 mol B.1.5 mol C.1.8 mol D.2.5 mol
C
解析:由题意知,平衡时n(CO2)=0.75 mol,则n(H2)=0.75 mol
所以n(H2)+n(CO2)=1.5 mol,再通入6 mol 水蒸气,平衡向生成CO2和H2方向移动,n(CO2)值增大,n(H2)?值也增大,但n(CO2)最大值小于1 mol,n(H2)=n(CO2)<1 mol,所以n(H2)+n(CO2)<2 mol
故1.5 mol<n(H2)+n(CO2)<2 mol,故选C。

练习册系列答案
相关题目
在一定温度下,将CO和水蒸汽各1mol放在密闭容器中反应: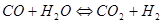 ,达平衡后测得
,达平衡后测得 为0.6mol,再通入4mol水蒸汽,达新的平衡后,
为0.6mol,再通入4mol水蒸汽,达新的平衡后, 物质的量
物质的量
| A.等于0.6mol | B.等于1mol |
| C.大于0.6mol,小于1mol | D.大于1mol |

 ,达平衡后测得
,达平衡后测得 为0.6mol,再通入4mol水蒸汽,达新的平衡后,
为0.6mol,再通入4mol水蒸汽,达新的平衡后,