题目内容
向溴水中加入足量的乙醛溶液,可以看到溴水褪色.对产生该现象的原因有如下三种猜想;①溴水与乙醛发生取代反应:②由于乙醛分子中有不饱和键,溴水与乙醛发生加成反应;③由于乙醛具有还原性,溴水将乙醛氧化为乙酸,为探究哪一种猜想正确.某研究性学习小组提出了如下两种实验方案:
实验方案一:检验褪色后溶液的酸碱性.
实验方案二:测定反应前后溴水中Br2的物质的量和反应后Br-的物质的是
(1)方案一是否可行? ,理由是
(2)假设测得反应前溴水中Br2的物质的量为a mol,若测得反应后n(Br-)= mol.说明溴水与乙醛发生取代反应;若测得反应后n(Br-)= mol,说明溴水与乙醛发生加成反应;若测得反应后
n(Br-)= mol,说明溴水将醛氧化为乙酸.
(3)按物质的量之比为1:5配制成1000mL KBrO3-KBr溶液,该溶液在酸性条件下完全反应可生成0.5mol Br2,取该溶液10mL,加入足量乙醛溶液使其褪色,然后将所得溶液稀释为100mL,准确取其中的10mL,加入过量AgNO3溶液,过滤、洗涤、干燥后称量得到固体0.188g.若已知COOAg易溶于水,试通过计算判断溴水与乙醛发生反应的类型为 (填序号)
①取代反应 ②加成反应 ③氧化反应
(4)写出上述测定过程中反应的离子方程式
①KBrO3与KBr在酸性条件下的反应
②溴水与乙醛反应
(5)根据上述信息,试推测向酸性KMnO4溶液中滴加乙醛可能出现的现象: .
实验方案一:检验褪色后溶液的酸碱性.
实验方案二:测定反应前后溴水中Br2的物质的量和反应后Br-的物质的是
(1)方案一是否可行?
(2)假设测得反应前溴水中Br2的物质的量为a mol,若测得反应后n(Br-)=
n(Br-)=
(3)按物质的量之比为1:5配制成1000mL KBrO3-KBr溶液,该溶液在酸性条件下完全反应可生成0.5mol Br2,取该溶液10mL,加入足量乙醛溶液使其褪色,然后将所得溶液稀释为100mL,准确取其中的10mL,加入过量AgNO3溶液,过滤、洗涤、干燥后称量得到固体0.188g.若已知COOAg易溶于水,试通过计算判断溴水与乙醛发生反应的类型为
①取代反应 ②加成反应 ③氧化反应
(4)写出上述测定过程中反应的离子方程式
①KBrO3与KBr在酸性条件下的反应
②溴水与乙醛反应
(5)根据上述信息,试推测向酸性KMnO4溶液中滴加乙醛可能出现的现象:
考点:探究化学反应机理,乙醛的化学性质,探究对经典问题的质疑
专题:实验探究和数据处理题
分析:(1)检验褪色后溶液的酸碱性不能确定是取代反应还是氧化反应;
(2)若发生取代反应,1molBr2可生成1molHBr;若发生加成反应,则无HBr生成;若发生氧化反应,1molBr2可被还原生成2molHBr;
(3)根据计算判断反应类型;
(4)根据氧化还原反应的规律进行书写;
(5)酸性KMnO4溶液具有强氧化性,乙醛具有还原性.
(2)若发生取代反应,1molBr2可生成1molHBr;若发生加成反应,则无HBr生成;若发生氧化反应,1molBr2可被还原生成2molHBr;
(3)根据计算判断反应类型;
(4)根据氧化还原反应的规律进行书写;
(5)酸性KMnO4溶液具有强氧化性,乙醛具有还原性.
解答:
解:(1)因溴水与乙醛发生取代反应有HBr生成;乙醛被氧化生成乙酸和HBr,溶液均呈酸性,故不能用测定溶液酸碱性的方法,方案一不可行,
故答案为:不可行;溴水与乙醛发生取代反应和乙醛被溴水氧化都有溴化氢生成,溶液均显酸性;
(2)若发生取代反应,1molBr2可生成1molHBr,故反应后n(Br-)=amol;若发生加成反应,则无HBr生成,故反应后n(Br-)=0;若发生氧化反应,1molBr2可被还原生成2molHBr,故反应后n(Br-)=2amol,
故答案为:a;0;2a;
(3)与乙醛反应的Br2为0.5×
=0.005mol:n(AgBr)=
=0.001mol,故Br2与乙醛反应生成的Br-为:0.001mol×
=0.01mol,故n(Br-):n(Br2)=0.01:0.005=2:1,故发生氧化反应,
故答案为:③;
(4)①KBrO3与KBr在酸性条件下发生氧化还原反应,生成单质溴,方程式为:BrO3-+5Br-+6H+=3Br2+3H2O,
故答案为:BrO3-+5Br-+6H+=3Br2+3H2O;
②溴水与乙醛发生氧化还原反应,方程式为:CH3CHO+Br2+H2O=CH3COOH+2H++2Br-,
故答案为:CH3CHO+Br2+H2O=CH3COOH+2H++2Br-;
(5)乙醛能与酸性KMnO4溶液发生氧化还原反应,从而使酸性KMnO4溶液褪色,
故答案为:溶液的紫色褪去.
故答案为:不可行;溴水与乙醛发生取代反应和乙醛被溴水氧化都有溴化氢生成,溶液均显酸性;
(2)若发生取代反应,1molBr2可生成1molHBr,故反应后n(Br-)=amol;若发生加成反应,则无HBr生成,故反应后n(Br-)=0;若发生氧化反应,1molBr2可被还原生成2molHBr,故反应后n(Br-)=2amol,
故答案为:a;0;2a;
(3)与乙醛反应的Br2为0.5×
| 10 |
| 1000 |
| 0.188g |
| 188g/mol |
| 100 |
| 10 |
故答案为:③;
(4)①KBrO3与KBr在酸性条件下发生氧化还原反应,生成单质溴,方程式为:BrO3-+5Br-+6H+=3Br2+3H2O,
故答案为:BrO3-+5Br-+6H+=3Br2+3H2O;
②溴水与乙醛发生氧化还原反应,方程式为:CH3CHO+Br2+H2O=CH3COOH+2H++2Br-,
故答案为:CH3CHO+Br2+H2O=CH3COOH+2H++2Br-;
(5)乙醛能与酸性KMnO4溶液发生氧化还原反应,从而使酸性KMnO4溶液褪色,
故答案为:溶液的紫色褪去.
点评:本题考查化学实验方案的评价,题目难度中等,注意根据反应的类型判断反应可能的产物,把握实验原理.

练习册系列答案
相关题目
科学家P.Tatapudi等人首先使用在空气中电解纯水(酸性条件下)的方法制得臭氧.同时还得到了过氧化氢,下列电极反应式正确的是( )
| A、阳极反应:3O2+6H++6e-=3H2O2 |
| B、阳极反应:3H2O一6e-=O3+6H+ |
| C、阴极反应:3O2+6H2O+6e-=3H2O2+6OH- |
| D、阴极反应:3H2O一6e-=O3+6H+ |
下列说法不正确的是( )
| A、霾的形成与PM2.5有直接关系 |
| B、自行车钢架生锈主要是电化学腐蚀所致 |
| C、用加热的方法杀死H7N9禽流感病毒是采用了蛋白质变性原理 |
| D、人类在研究物质微观结构的过程中,扫描隧道显微镜、光学显微镜、电子显微镜先后得到了使用 |
部分弱酸的电离平衡常数如表,表述肯定正确的是( )
| 弱酸 | H2CO3 | H2SO3 | HClO |
| 电离平衡常数 (25℃) |
K1=4.30×10-7 | K1=1.54×10-2 | K=2.95×10-8 |
| K2=5.61×10-11 | K2=1.02×10-7 |
| A、相同温度时三种溶液的pH关系:Na2CO3>NaClO>Na2SO3 |
| B、ClO-+H2O+CO2→HClO+HCO3- |
| C、2ClO-+SO2+H2O→2HClO+SO32- |
| D、等体积、等物质的量浓度的HClO 和Na2CO3混合后溶液呈碱性 |
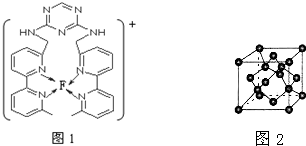 现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期.B元素含有3个能级,且每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子.请回答下列问题:
现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期.B元素含有3个能级,且每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子.请回答下列问题: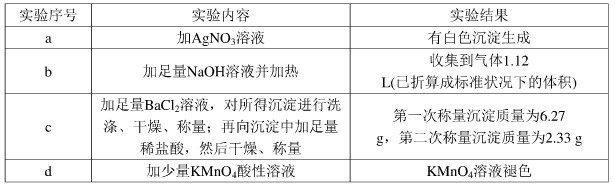
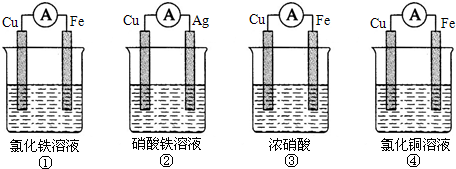
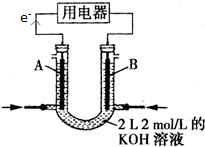
 已知溶液中,还原性为HSO3->I-,氧化性为IO3->I2>SO42-.
已知溶液中,还原性为HSO3->I-,氧化性为IO3->I2>SO42-.