题目内容
1molCxHy(烃)完全燃烧需要5molO2,则X与Y之和可能是( )
| A、X+Y=5 |
| B、X+Y=7 |
| C、X+Y=11 |
| D、X+Y=9 |
考点:有关有机物分子式确定的计算,化学方程式的有关计算
专题:计算题
分析:1mol烃CxHy耗氧量为(x+
)mol,据此判断.
| y |
| 4 |
解答:
解:1mol某气态烃CxHy完全燃烧,需用5mol O2,所以(x+
)mol=5mol.
当x=3、y=8,则x+
=5,即X+Y=11,
当x=4、y=4,则x+
=5,即X+Y=8,
故选C.
| y |
| 4 |
当x=3、y=8,则x+
| y |
| 4 |
当x=4、y=4,则x+
| y |
| 4 |
故选C.
点评:本题考查了烃的燃烧规律,根据有机物耗氧量判断有机物分子式,难度不大,关键根据耗氧量讨论可能组成.

练习册系列答案
相关题目
下列有关实验装置进行的相应实验,不能达到实验目的是( )
A、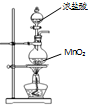 用装置制取氯气 |
B、 用装置除去氯气中的少量氯化氢和水蒸气 |
C、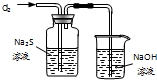 用装置可证明Cl2的氧化性强于S |
D、 用装置可以完成“喷泉”实验 |
相同物质的量的下列有机物,充分燃烧,消耗氧气量相同的是( )
| A、C3H4和C2H6 |
| B、C3H6和C4H8O |
| C、C3H6O2和C3H8O |
| D、C3H8O和C4H6O2 |
甲、乙、丙、丁都是短周期元素,其中甲、丁在周期表中的相对位置如表,甲原子最外层电子数是其内层电子数的2倍,乙单质在空气中燃烧发出黄色火焰,丙是地壳中含量最高的金属元素.下列判断正确的是( )
| 甲 | |||
| 丁 |
| A、原子半径:丙>丁 |
| B、甲与丁的核外电子数相差10 |
| C、氢氧化物碱性:乙>丙 |
| D、甲、乙的最高价氧化物均是共价化合物 |

 ,请写出其涉及的反应(注明反应的条件
,请写出其涉及的反应(注明反应的条件
