题目内容
9.某些电解质分子的中心原子最外层不足8电子,其电离时结合其他离子使中心原子最外层达到8电子结构.例如硼酸在水中电离方程式为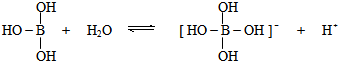 .下列判断正确的是( )
.下列判断正确的是( )| A. | 硼酸是三元酸,抑制水的电离 | |
| B. | 硼酸分子中各原子最外层均达到8电子结构 | |
| C. | 硼酸与NaOH溶液反应的离子方程式:H3BO3+OH-═[B(OH)4]- | |
| D. | 硼酸是两性氢氧化物,也能与强酸溶液反应 |
分析 A、硼酸的电离结合了水溶液中的氢氧根离子;
B、H原子最外层可达到2电子稳定结构;
C、硼酸能和OH-发生化合反应,而使中心原子最外层电子达到饱和结构.
D、硼酸是酸,电离出的阳离子全部是氢离子.
解答 解:A、硼酸在水中的电离过程为: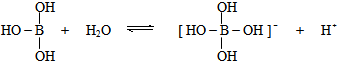 ,可以看出硼酸的电离结合了水溶液中的氢氧根离子,对水的电离起促进作用,故A错误;
,可以看出硼酸的电离结合了水溶液中的氢氧根离子,对水的电离起促进作用,故A错误;
B、B原子最外层达到8电子结构,H原子最外层达到2电子稳定结构,故B错误;
C、硼酸能和OH-发生化合反应,而使中心原子最外层电子达到饱和结构,即:H3BO3+OH-=[B(OH)4]-,故C正确;
D、硼酸电离出的阳离子全部是氢离子,属于酸,不是两性氢氧化物,故D错误.
故选C.
点评 本题考查弱电解质在水溶液中的电离,正确获取信息并利用信息解答问题是解本题关键,侧重考查学生自学及知识迁移能力,题目难度中等.

练习册系列答案
相关题目
19.已知a、b、c是中学常见的含有同种元素的三种物质,具有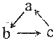 的转化关系(“→”表示在一定条件下可一步完成),下列各组物质中,不符合上述转化关系的是( )
的转化关系(“→”表示在一定条件下可一步完成),下列各组物质中,不符合上述转化关系的是( )
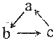 的转化关系(“→”表示在一定条件下可一步完成),下列各组物质中,不符合上述转化关系的是( )
的转化关系(“→”表示在一定条件下可一步完成),下列各组物质中,不符合上述转化关系的是( )| 选项 对应物质 | A | B | C | D |
| a | Cu(OH)2 | NO | Fe | Al |
| b | CuCl2 | NO2 | FeCl3 | Al(OH)3 |
| c | Cu | HNO3 | FeCl2 | AlO2- |
| A. | A | B. | B | C. | C | D. | D |
20.必须随配随用,不能长期存放的试剂是( )
| A. | 氢硫酸 | B. | 盐酸 | C. | AgNO3溶液 | D. | NaOH溶液 |
17.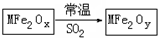 新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中化合价不变化.常温下,MFe2Ox能使工业废气中的SO2转化为S,转化过程表示如图.下列说法正确的是( )
新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中化合价不变化.常温下,MFe2Ox能使工业废气中的SO2转化为S,转化过程表示如图.下列说法正确的是( )
 新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中化合价不变化.常温下,MFe2Ox能使工业废气中的SO2转化为S,转化过程表示如图.下列说法正确的是( )
新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中化合价不变化.常温下,MFe2Ox能使工业废气中的SO2转化为S,转化过程表示如图.下列说法正确的是( )| A. | x<y | B. | SO2是该反应的催化剂 | ||
| C. | MFe2Ox是还原剂 | D. | 氧化性:MFe2Oy>SO2 |
4.室温下由水电离出的H+的浓度是1×10-12mol/L,则该溶液( )
| A. | 可能是酸性溶液 | B. | 可能是碱性溶液 | C. | 可能是中性溶液 | D. | 不能判断 |
14.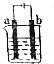 如图a、b均为铂电极,电解一段时间后,烧杯中溶液的pH增大,则选用的电解质溶液可以是( )
如图a、b均为铂电极,电解一段时间后,烧杯中溶液的pH增大,则选用的电解质溶液可以是( )
 如图a、b均为铂电极,电解一段时间后,烧杯中溶液的pH增大,则选用的电解质溶液可以是( )
如图a、b均为铂电极,电解一段时间后,烧杯中溶液的pH增大,则选用的电解质溶液可以是( )| A. | H2SO4溶液 | B. | NaCl溶液 | C. | AgNO3溶液 | D. | KOH溶液 |
1.下列在水溶液中能大量共存的离子组是( )
| A. | K+,Mg2+,Cl-,OH- | B. | Na+,Cu2+,CO32-,NO3- | ||
| C. | H+,Na+,CO32-,Cl- | D. | Na+,Mg2+,Cl-,SO42- |
11.下列各组物质中,互为同分异构体的是( )
| A. | O2与O3 | B. | ${\;}_{6}^{14}$C与${\;}_{6}^{12}$C | ||
| C. | CH2Cl2与CHCl3 | D. | CH3-CH2-CH2-CH3与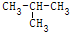 |