题目内容
7.制备溴苯的实验装置如图,将液溴从恒压滴液漏斗慢慢滴入盛有苯和铁粉的烧瓶A.反应结束后,对A中的液体进行后续处理即可获得溴苯.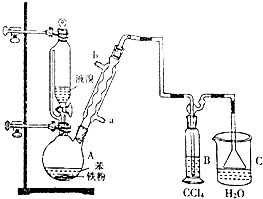
(1)在反应中实际起催化作用的是FeBr3,写出A中发生的所有化学反应方程式
 .
.(2)已知上述有机反应放出大量热,则A中的现象是反应液微沸及有红棕色气体充满A容器.
(3)冷凝管的作用是冷凝回流,冷凝管中的水应从a口进入(填“a”或“b”).B中盛放的CCl4的作用是除去溴化氢气体中的溴蒸气.
(4)向C中加入硝酸银溶液可证明苯和液溴发生的是取代反应不是加成反应,反应现象是有淡黄色沉淀生成.也可使用蓝色石蕊试纸更简便地证明上述结论.
(5)得到粗溴苯后,要用如下操作精制:①蒸馏 ②水洗 ③用干燥剂干燥 ④10%NaOH溶液洗,正确的操作顺序是b(填字母标号).
a.①②③④②b.②④②③①c.④②③①②d.②④①②③
分析 根据实验装置图可知,在装置A中用苯与溴在铁粉作催化剂的条件下生成溴苯和溴化氢,由于苯和液溴都是易挥发的物质,为了提高原料的利用率,用球形冷凝管进行冷凝回流,生成的溴化氢气体中含有少量的溴蒸,用B装置中的四氯化碳除去溴化氢中的溴蒸汽,在装置C中用水吸收生成的溴 化氢,由于溴化氢极易溶于水,所以在用水吸收溴化氢的时候用防倒吸装置.
(1)A中用苯与溴在铁粉作催化剂的条件下生成溴苯和溴化氢;
(2)该反应为放热反应,苯和液溴均易挥发,溴蒸气是一种红棕色的气体,据此分析解答;
(3)采用冷凝管的作用是将挥发出的反应物蒸气冷凝使其回流到反应容器中;冷凝水的水流方向和气流方向相反,逆流冷凝效果好,需下口进,上口出;溴极易溶于四氯化碳,
B中盛放的CCl4的作用是除去溴化氢气体中的溴蒸气;
(4)根据上面的分析可知,C中是用水吸收的溴化氢,能与硝酸银溶液反应生成浅黄色沉淀,溴化氢溶液呈酸性能使石蕊试纸变红;
(5)得到粗溴苯中含有苯、溴、溴化铁等杂质,要先用水洗除溴化铁,再用碱洗除溴,再水洗除碱等,再干燥、蒸馏除苯,据此答题.
解答 解:(1)A中用苯与溴在铁粉作催化剂的条件下反应,苯环上的一个氢原子被一个溴原子取代,其反应方程式为: ,
,
故答案为: ;
;
(2)由于反应放热,反应液微沸,苯和液溴均易挥发,溴蒸气是一种红棕色的气体,有红棕色气体充满A容器,
故答案为:反应液微沸;有红棕色气体充满A容器;
(3)溴与苯发生取代反应生成溴苯与溴化氢,反应放热,冷凝管的作用是冷凝挥发出来的苯和液溴,并使它们流回到烧瓶中,冷凝水的水流方向和气流方向相反,下口进,上口出,所以加热A前,需先从“a”口通入水,克服水的重力充满冷凝管,与气体逆流,冷凝效果好,根据相似相溶原理,溴极易溶于四氯化碳,而溴化氢则不溶,所以C中盛放CCl4的作用是除去溴化氢气体中的溴蒸气,
故答案为:冷凝回流;a;除去溴化氢气体中的溴蒸气;
(4)证明苯和液溴发生的是取代反应而不是加成反应,即证明有溴化氢产生即可,所以加入硝酸银溶液后溶液中有浅黄色沉淀产生,或者用蓝色石蕊试纸检验溴化氢的存在,
故答案为:有淡黄色沉淀生成;蓝色石蕊;
(5)得到粗溴苯中含有苯、溴、溴化铁等杂质,要先用水洗除溴化铁,再用碱洗除溴,再水洗除碱等,再干燥、蒸馏除苯,所以实验的正确的操作顺序是②④②③①,
故答案为:b.
点评 本题考查有机物实验制备,涉及溴苯的制取,侧重考查学生对装置与原理的分析评价,明确各个装置的作用及基本操作方法,题目难度中等.

| A. | 乙烯使酸性KMnO4溶液褪色 | |
| B. | 乙烯使溴水褪色 | |
| C. | 点燃乙烯出现黑烟 | |
| D. | 甲烷与氯气的混合气体,光照一段时间后褪色 |
| A. | 已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ•mol-1,则含20.0 g NaOH的稀溶液与稀醋酸完全中和,放出的热量小于28.65kJ | |
| B. | 已知2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ•mol-1,则标况下1mol氢气完全燃烧放出241.8 kJ的热量 | |
| C. | 已知2C(s)+2O2(g)=2CO2(g)△H=a kJ•mol-1,2C(s)+O2(g)=2CO(g)△H=b kJ•mol-1,则a>b | |
| D. | 已知P (白磷,s)=P (红磷,s)△H<0,则白磷比红磷稳定 |
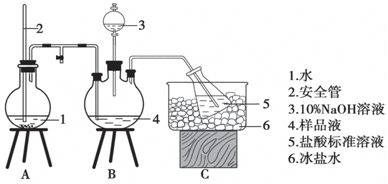 某小组以CoCl2•6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X.为确定其组成,进行如下实验.
某小组以CoCl2•6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X.为确定其组成,进行如下实验.①氨的测定:精确称取w g X,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1 mL c1 mol•L-1的盐酸标准溶液吸收.蒸氨结束后取下接收瓶,用c2 mol•L-1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液.
②氯的测定
回答下列问题:
(1)装置中安全管的作用原理是使A瓶中压强稳定.
(2)用NaOH标准溶液滴定过剩的HCl时,应使用碱式滴定管,可使用的指示剂为酚酞或甲基橙.
(3)样品中氨的质量分数表达式为$\frac{(C{\;}_{1}V{\;}_{1}-C{\;}_{2}V{\;}_{2})×10{\;}^{-3}×17}{w}$×100%.
(4)测定氨前应该对装置进行气密性检查,若气密性不好测定结果将偏低(填“偏高”或“偏低”).
(5)氯的测定采用莫尔法,莫尔法是一种沉淀滴定法,用标准硝酸银溶液滴定,进行测定溶液中Cl-的浓度.已知:
| 银盐 性质 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
| 溶解度(mol•L-1) | 1.3410-6 | 7.110-7 | 1.110-8 | 6.510-5 | 1.010-6 |
A.NaCl B.BaBr2 C.Na2CrO4 D.KSCN
②滴定终点的现象是滴入最后一滴标准溶液,生成砖红色沉淀,且30s 不复原.
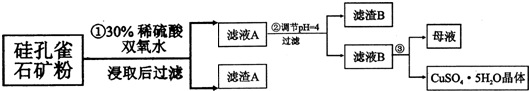
(1)步骤1中先加入足量稀硫酸,再加人双氧水.则双氧水参与该反应的离子方程式是2Fe2++H2O2+2H+═2Fe3++2H2O.
(2)步骤②调节溶液pH,可以选用的试剂是BC.(填字母编号)
A.A12O3 B.CuO C.CuCO3•Cu(OH)2
(3)有关氢氧化物开始沉淀和完全沉淀的pH如下表:
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 |
(4)将滤液B通过蒸发浓缩、冷却结晶、过滤等操作可得到硫酸铜晶体.
(5)硫酸铜也可用硫化铜和氧气在高温、催化剂条件下化合制得,该反应的化学方程式是CuS+2O2$\frac{\underline{\;\;\;高温\;\;\;}}{催化剂}$CuSO4.取384g CuS在一定条件下和氧气完全反应,若发生2CuS+3O2=2CuO+2SO2和4CuS+5O2=2Cu2O+4SO2两个反应,在所得固体中Cu和O的物质的量之比n(Cu):n(O)=4:a,此时消耗空气的物质的量为bmol.则a=$\frac{2}{5}$b-8.(氧气占空气体积的五分之一)