题目内容
6.下列水解方程式的书写中,正确的是( )| A. | CH3COO-的水解方程式:CH3COO-+H2O?CH3COOH+OH- | |
| B. | HCO3-的水解方程式:HCO3-+H2O?CO32-+H3O+ | |
| C. | CO32-的水解方程式:CO32-+2H2O?H2CO3+2OH- | |
| D. | Fe3+的水解方程式:Fe3++3OH-?Fe(OH)3 |
分析 A.水解生成醋酸和氢氧根离子;
B.水解生成碳酸和氢氧根离子;
C.水解分步进行,以第一步为主;
D.水解生成氢氧化铁和氢离子.
解答 解:A.CH3COO-的水解方程式为CH3COO-+H2O?CH3COOH+OH-,故A正确;
B.HCO3-的水解方程式为HCO3-+H2O?H2CO3+OH-,故B错误;
C.CO32-的水解方程式为CO32-+H2O?HCO3-+OH-,故C错误;
D.Fe3+的水解方程式为Fe3++3H2O?Fe(OH)3+3H+,故D错误;
故选A.
点评 本题考查离子方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重水解反应的离子反应考查,注意离子反应中保留化学式的物质及电荷守恒,题目难度不大.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
16.铝在人体中积累可使人慢性中毒,1989年世界卫生组织正式将铝确定为食品污染源之一,而加以控制.
铝在下列使用场合须加以控制的是①制铝锭②制易拉罐③制电线电缆④制牙膏皮⑤用明矾净水⑥制炊具⑦用明矾和苏打作食物膨化剂⑧用Al(OH)3制成药片治胃病⑨制防锈油漆( )
铝在下列使用场合须加以控制的是①制铝锭②制易拉罐③制电线电缆④制牙膏皮⑤用明矾净水⑥制炊具⑦用明矾和苏打作食物膨化剂⑧用Al(OH)3制成药片治胃病⑨制防锈油漆( )
| A. | ①②④⑤⑥⑦⑧ | B. | ②⑤⑥⑦⑨ | C. | ②④⑤⑥⑦⑧ | D. | ③④⑤⑥⑦⑧ |
1.下列物质能促进水的电离的是( )
| A. | HCl | B. | CH3COONa | C. | NaOH | D. | NaCl |
18.如图表示某反应的能量变化,对于该图的理解,你认为一定正确的是( )
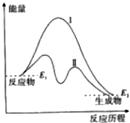

| A. | 曲线Ⅰ和曲线Ⅱ分别表示两个化学反应的能量变化 | |
| B. | 曲线Ⅱ可表示反应2NH3$?_{高温高压}^{催化剂}$N2+3H2的能量变化 | |
| C. | 该反应不需要加热就能发生 | |
| D. | 该反应的△H=E2-E1 |
16.某恒容密闭容器中充入等物质的量的A 和B,一定温度下发生反应A(s)+xB(g)?2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:
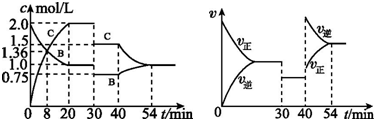
下列说法中正确的是( )

下列说法中正确的是( )
| A. | 30 min~40 min 间该反应使用了催化剂 | |
| B. | 反应方程式中的x=2,正反应为吸热反应 | |
| C. | 30 min 时条件的变化是降低压强,40 min 时条件的变化是升高温度 | |
| D. | 前8 min A 的平均反应速率为0.08 mol•L-1•min-1 |
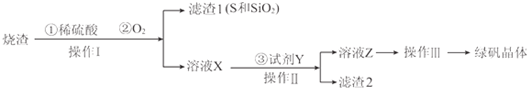
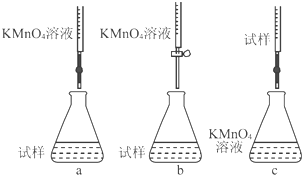

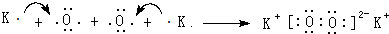 (用元素符号表示).
(用元素符号表示).