题目内容
在同温同压下,下列各组热化学方程式中,△H2>△H1的是( )
| A、2H2(g)+O2(g)═2H2O(g)△H1; 2H2(g)+O2(g)═2H2O(l)△H2 | ||
| B、S(g)+O2(g)═SO2(g)△H1; S(s)+O2(g)═SO2(g)△H2 | ||
C、CO(g)+
| ||
| D、C(s)+H2O(g)═CO(g)+H2(g)△H1;CaO(s)+H2O(l)═Ca(OH)2(s)△H2 |
考点:反应热的大小比较
专题:化学反应中的能量变化
分析:A.液态水变为气态水的过程是吸热过程;
B.固体硫变为气态硫需要吸收热量;
C.焓变数值与方程式的系数成正比,化学反应方程式的系数加倍,焓变数值加倍;
D.前者为吸热反应,后者为放热反应.
B.固体硫变为气态硫需要吸收热量;
C.焓变数值与方程式的系数成正比,化学反应方程式的系数加倍,焓变数值加倍;
D.前者为吸热反应,后者为放热反应.
解答:
解:A.物质的燃烧反应是放热的,焓变是负值,液态水变为气态水的过程是吸热的,故△H1>△H2,故A错误;
B.物质的燃烧反应是放热的,所以焓变是负值,固体硫变为气态硫需要吸收热量,所以△H1<△H2,故B正确;
C.化学反应方程式的系数加倍,焓变数值加倍,该化合反应是放热的,所以焓变值是负值,△H2=2△H1,△H1>△H2,故C错误;
D.C(s)+H2O(g)═CO(g)+H2(g)为吸热反应,△H1>0,CaO(s)+H2O(l)═Ca(OH)2(s)为放热反应,△H2<0,故△H1>△H2,故D错误;
故选:B.
B.物质的燃烧反应是放热的,所以焓变是负值,固体硫变为气态硫需要吸收热量,所以△H1<△H2,故B正确;
C.化学反应方程式的系数加倍,焓变数值加倍,该化合反应是放热的,所以焓变值是负值,△H2=2△H1,△H1>△H2,故C错误;
D.C(s)+H2O(g)═CO(g)+H2(g)为吸热反应,△H1>0,CaO(s)+H2O(l)═Ca(OH)2(s)为放热反应,△H2<0,故△H1>△H2,故D错误;
故选:B.
点评:本题考查了物质反应能量变化分析判断,解题时注意物质的物质的量、聚集状态、产物对反应的能量变化的影响,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
化学与社会、生产、生活紧切相关,下列说法正确的是( )
| A、为了治理酸雨污染,政府应取缔硫酸厂、火电厂、水泥厂等 |
| B、我国是稀土储量大国,可以大量开采稀土矿卖给全世界,赚取外汇 |
| C、减少燃煤的使用,改用风能、太阳能等能源,符合“低碳生活”理念 |
| D、由铝土矿(主要含Al2O3,还含有Fe2O3、SiO2等杂质)冶炼金属铝的过程中,只涉及复分解反应 |
某有机物的结构简式为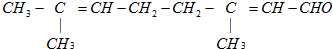 该有机物不可能发生的化学反应是( )
该有机物不可能发生的化学反应是( )
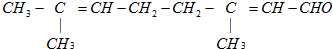 该有机物不可能发生的化学反应是( )
该有机物不可能发生的化学反应是( )| A、氧化 | B、酯化 | C、还原 | D、加成 |
下列有关有机物结构的叙述不正确的是( )
| A、一氟一氯甲烷只有一种结构,可以证明甲烷是正四面体结构 |
| B、乙烯和甲苯分子中所有原子都在同一个平面上 |
| C、邻二甲苯没有同分异构体表明苯的凯库勒结构式存在局限,不准确 |
D、 和CH3-CH═CH2互为同分异构体 和CH3-CH═CH2互为同分异构体 |
已知2A(g)?2B(g)+C(g)△H<0,在未用催化剂的条件下已达平衡,现要使正反应速率降低,c(B)减小,应采取的措施是( )
| A、升温 | B、增大反应器的体积 |
| C、增大c(A) | D、降温 |
2005年法拉利公司发布的敞篷车(法拉利Superam erica),其玻璃车顶采用了先进的电致变色系统,即在原来玻璃材料基础上增加了有电致变色系统组成的五层膜材料(如图所示).其工作原理是:在外接电源(外加电场)下,通过在膜材料内部发生氧化还原反应,实现对器件的光透过率进行多级可逆性调节,下列有关说法不正确的是( )


| A、当A接外接电源负极时,Li+脱离离子存储层 |
| B、当A接外接电源正极时,电致变色层发生反应为:LiWO3-e-=WO3+Li+ |
| C、当B接外接电源负极时,膜的透射率降低,可以有效阻挡阳光 |
| D、该电致变色系统在较长时间的使用过程中离子导体层中Li+的量可保持基本不变 |
下列反应属于取代反应的是( )
| A、CH2=CH2+Br2→CH2BrCH2Br | ||||
B、 | ||||
C、C16H34
| ||||
| D、2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ |
 如图所示的电解池I和Ⅱ中,a、b、c和d均为Pt电极.电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b>d.符合上述实验结果的盐溶液是( )
如图所示的电解池I和Ⅱ中,a、b、c和d均为Pt电极.电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b>d.符合上述实验结果的盐溶液是( )